您可能也喜欢
过去几年,以小核酸药物为代表的RNA疗法被寄予厚望。在精准医学时代,这类药物展现出巨大的潜力:能够直接调控基因表达,作用机制清晰,分子设计灵活。然而,目前已获批或进入临床应用的小核酸药物,几乎都集中在肝脏靶向这一条跑道上。
肝脏具备多重“天然优势”—血流丰富、吞吐能力高;肝细胞表面高度表达 ASGPR 受体,使 GalNAc 偶联策略得以成功;加之肝脏安全性与药代特征已有充分的数据积累。随着肝脏逐渐成为 RNA 递送的技术“舒适区”,其局限性也日益凸显。事实上,人体中约 80% 的致病基因在肝外组织中表达,包括神经系统疾病(如肌萎缩侧索硬化症ALS、阿尔茨海默 AD)、肌肉疾病(如杜氏肌营养不良症 DMD)、以及肺、肾、免疫系统相关疾病等。
要让小核酸药物真正释放潜力,它必须跳出肝脏,在更多组织中建立可控、有效的分布,实现真正意义上的多组织精准递送。
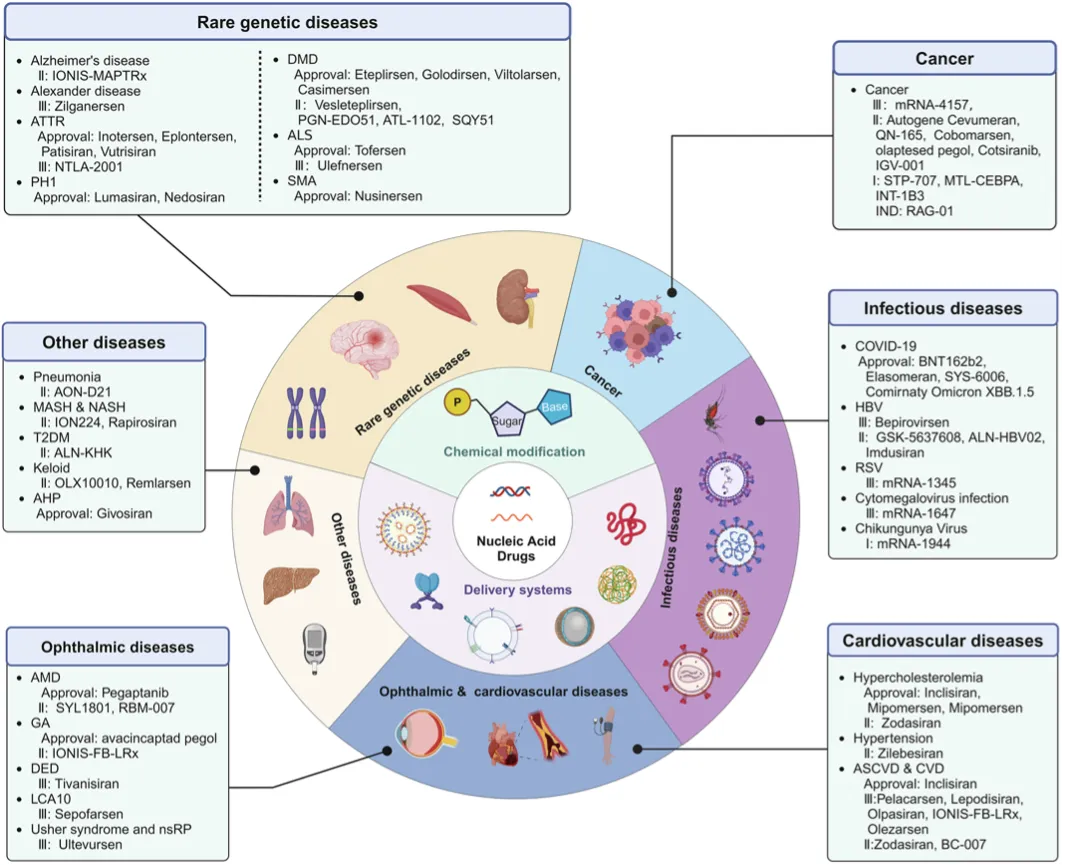
小核酸药物(NADs)已在少见遗传病、癌症、眼科、心血管及传染病等多领域进入临床或上市[1]
小核酸药物最早在罕见遗传病领域取得突破,并逐步拓展至癌症、眼科、心血管及传染病等多种疾病。与此同时,更广义的 RNA 与 DNA 类药物(如 mRNA 疫苗、DNA 疫苗与基因治疗)也在多个领域展现出显著疗效,共同推动精准医学的快速发展。
靶向肝外里程碑药物
● Nusinersen(Spinraza)
首个中枢神经系统 ASO 药物,通过鞘内注射调控 SMN2 基因剪接,用于治疗脊髓性肌萎缩症(SMA)。它的成功证明,只要能送达中枢神经系统,RNA 药物同样可以稳定发挥疗效。
● Eteplirsen(Exondys 51)
首个DMD外显子跳跃疗法,通过修复 DMD 基因阅读框,使患者重新产生部分功能性肌营养蛋白。
● Tofersen(Qalsody)
靶向 SOD1 基因的 ASO 药物,用于ALS,并于 2023 年获 FDA 加速批准,标志着 RNA 药物正式进军神经退行性疾病领域。
已经有越来越多的临床成果证明,小核酸药物肝外递送并非空谈,而是正在被验证的现实路径。
百奥赛图自主研发了肝外靶向小核酸药物模型小鼠,可用于系统评估药物在特定组织的疗效、靶向性及安全性,为相关疾病的小核酸药物临床前研究和开发提供可靠的实验平台,加速新药从发现到临床验证的进程。
中枢和外周神经系统
中枢神经系统(CNS)是神经退行性疾病的核心治疗靶点。这类疾病往往具有明确的遗传驱动或病理蛋白异常,但传统药物往往难以直接作用于病因,因此治疗手段长期受限。小核酸药物(如 ASO、siRNA、mRNA)通过靶向特定基因或调控 RNA 剪接,能够直接干预疾病的根源性机制,例如修复突变基因、降低有害蛋白表达或补充缺失蛋白,从而实现精准治疗。[2]
人TAU靶向小核酸药物对B-hTFR1/hTAU小鼠的抑制作用
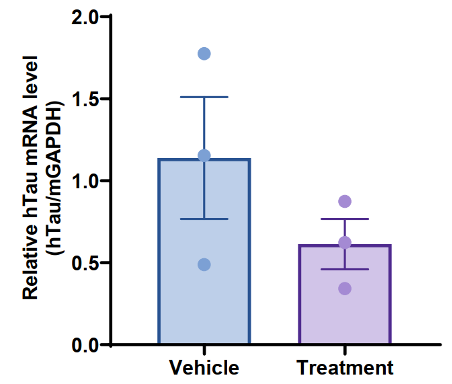
有关药物的具体信息,包括给药策略、剂量和用药时间尚未公开。此处仅分享客户允许披露的数据。
人 PMP22 靶向小核酸药物对 B-Tg(hPMP22) 小鼠的抑制效果
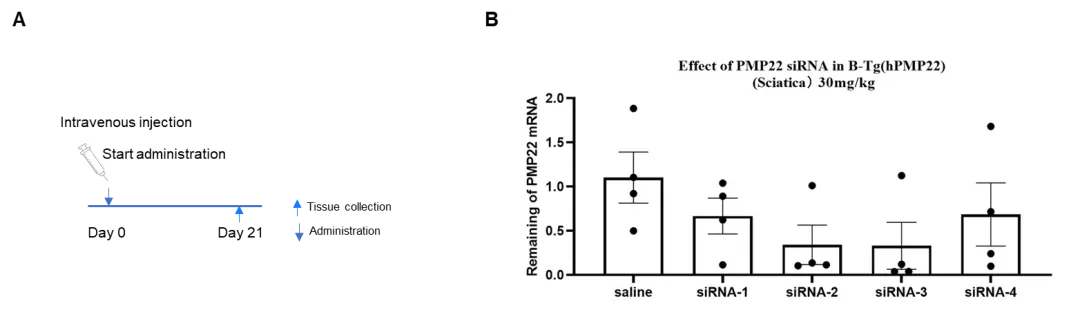
小核酸药物对 B-Tg(hPMP22) 小鼠体内人 PMP22 的抑制效果。在第 0 天,分别向 B-Tg(hPMP22) 小鼠给予人 PMP22 靶向小核酸药物(客户提供)和生理盐水。在第 21 天处死小鼠,收集坐骨神经组织,通过 qPCR 检测人 PMP22 mRNA 的表达水平。与对照组(生理盐水)相比,治疗组(siRNA)中的人 PMP22 mRNA 显著降低,这表明 B-Tg(hPMP22) 小鼠为体内评估人 PMP22 靶向核酸药物提供了强大的临床前模型。数据以平均值±标准误的形式表示。
注:本实验由客户使用 B-Tg(hPMP22) 小鼠开展,其他实验材料均由客户提供。
肌肉
小核酸药物在肌肉相关疾病治疗中展现出重要潜力,尤其在遗传性肌肉疾病如DMD和SMA中已取得突破性进展。通过ASO或siRNA技术,小核酸药物能够调控致病基因的表达或剪接,恢复关键蛋白功能,从而延缓疾病进展。多款ASO药物已获批用于临床,如Nusinersen(Spinraza)是通过 SMN2 剪接调控恢复肌肉功能;[3] Eteplirsen 在 DMD 患者中外显子跳跃及 Dystrophin 表达有显著提升(PROMOVI 96 周结果)。[4] 随着递送系统(如脂质纳米颗粒、抗体偶联载体)的优化,小核酸药物有望进一步拓展至其他肌营养不良症和肌肉萎缩性疾病,成为精准肌肉疾病治疗的重要方向。
抗体寡核苷酸偶联药物对人DMPK的抑制效果
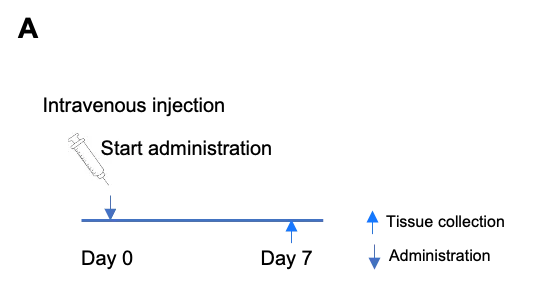
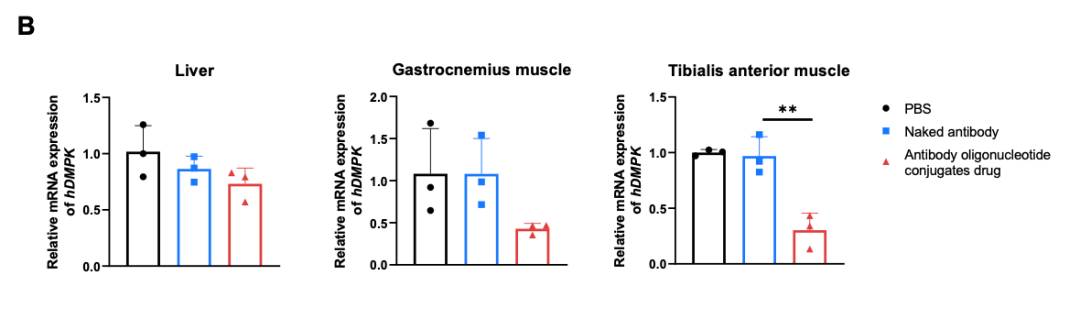
抗体-寡核苷酸偶联药物对杂合B-hTFR1/hDMPK小鼠DMPK的抑制效果。抗体寡核苷酸偶联药物(内部合成)、裸抗体(内部合成)和PBS分别于第0天给药于杂合B-hTFR1/hDMPK小鼠。第7天处死小鼠,取肝脏、腓肠肌和胫前肌,采用qPCR检测人DMPK mRNA的表达水平。与对照组(裸抗体和PBS)相比,治疗组(抗体寡核苷酸偶联药物)在胫骨前肌中的人DMPK mRNA显著降低,表明B-hTFR1/hDMPK小鼠为体内评价人DMPK靶向抗体寡核苷酸偶联药物提供了强有力的临床前模型。数值以平均值±SEM表示。
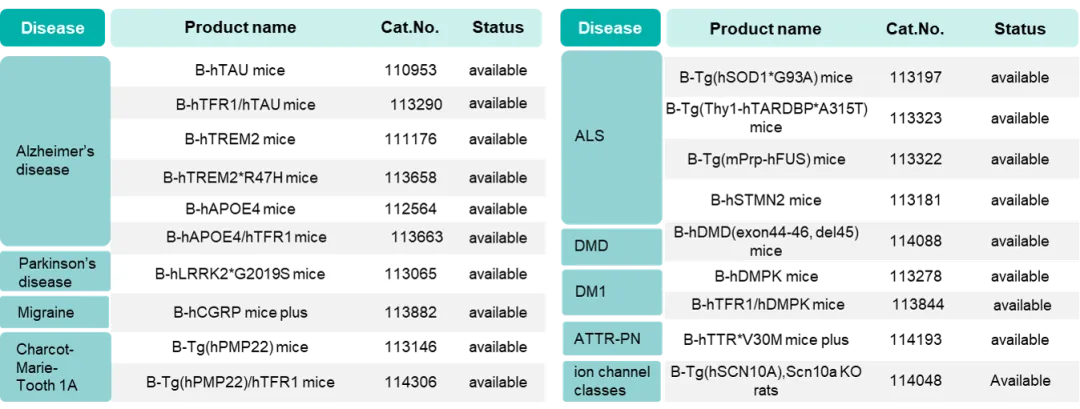
神经&肌肉小核酸药物相关产品列表
肺部
肺部疾病是小核酸药物的一个重要肝外靶点。通过局部吸入、化学修饰和纳米载体策略,RNA 和 ASO 药物能够直接调控肺组织基因表达,改善病理功能,显示出对囊性纤维化、哮喘及呼吸道病毒感染等疾病的潜在治疗价值。[5] 未来,随着递送技术和药物优化升级,肺部小核酸疗法有望成为精准肺病治疗的重要手段。
RAGE靶向核酸药物对B-hRAGE plus小鼠的抑制效果
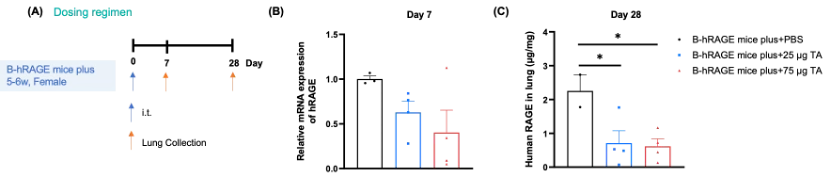
RAGE 靶向小核酸药物在 B-hRAGE plus纯合小鼠中的抑制效率。B-hRAGE plus小鼠(5–6 周龄,雌性)被随机分为 6 组。分别给小鼠注射人RAGE靶向核酸药物(客户提供)和PBS。核酸药物以PBS水溶液形式给药。小鼠于气道给药后第 7 天和第 28 天被处死。(A) 实验流程示意图。(B) 给药第 7 天肺组织中 RAGE mRNA 表达水平变化,与给药前水平比较。(C) 给药第 28 天肺组织中RAGE 蛋白表达变化。数据以平均值 ± SEM 表示,通过单因素方差分析(one-way ANOVA)进行统计,*P<0.05。
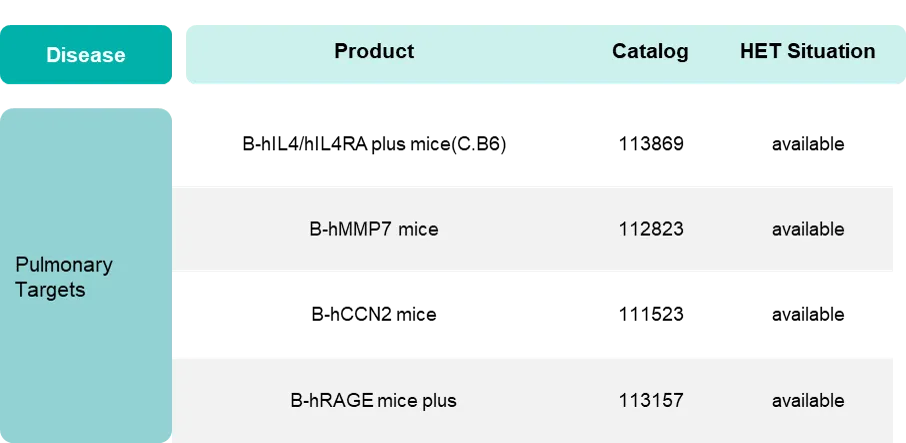
肺部疾病小核酸药物相关产品列表
参考文献:
1.Sun X, Setrerrahmane S, Li C, Hu J, Xu H. Nucleic acid drugs: recent progress and future perspectives. Signal Transduct Target Ther. 2024 Nov 29;9(1):316. doi: 10.1038/s41392-024-02035-4. PMID: 39609384; PMCID: PMC11604671.
2.Ou, K., et al. "Application of antisense oligonucleotide drugs in neurodegenerative diseases." Frontiers in Neuroscience 2025.
3.Greig SL. Obiltoxaximab: First Global Approval. Drugs. 2016 May;76(7):823-30. doi: 10.1007/s40265-016-0577-0. PMID: 27085536.
4.McDonald CM, Shieh PB, Abdel-Hamid HZ, Connolly AM, Ciafaloni E, Wagner KR,Goemans N, Mercuri E, Khan N, Koenig E, Malhotra J, Zhang W, Han B, Mendell JR;the Italian DMD Telethon Registry Study Group, Leuven NMRC Registry Investigators, CINRG Duchenne Natural History Investigators, and PROMOVI Trial Clinical Investigators. Open-Label Evaluation of Eteplirsen in Patients with Duchenne Muscular Dystrophy Amenable to Exon 51 Skipping: PROMOVI Trial. J Neuromuscul Dis. 2021;8(6):989-1001. doi: 10.3233/JND-210643. PMCID: PMC8673535.
5.Michael YT Chow, Yingshan Qiu, Jenny KW Lam , Inhaled RNA Therapy: From Promise to Reality, 2020 Sep 4;41(10):715–729. doi: 10.1016/j.tips.2020.08.002