在此页面上
细胞治疗是将活细胞输注到患者体内,以治疗或治愈疾病,可使用患者自身的细胞(自体)或来自供体的细胞(异体)。其中,免疫细胞疗法,尤其是CAR-T疗法,已在癌症治疗领域带来变革性突破,在血液系统恶性肿瘤中取得了显著成果。CAR-T细胞是一类经过工程改造的T细胞,能够表达嵌合抗原受体(CAR),从而识别并攻击肿瘤相关抗原。
百奥赛图提供先进的药理药效平台,支持多种细胞治疗的研发,包括CAR-T、CAR-Macrophages、CAR-NK、肿瘤浸润淋巴细胞(TILs)以及TCR-T等,覆盖体外实验服务与体内动物模型的完整研究流程。我们已建立一系列免疫缺陷小鼠模型,并构建了CDX模型及人源免疫系统重建模型,用于细胞治疗药物的体内药效评估与机制研究。
| Efficacy | MOA | Safety |
|
|
|
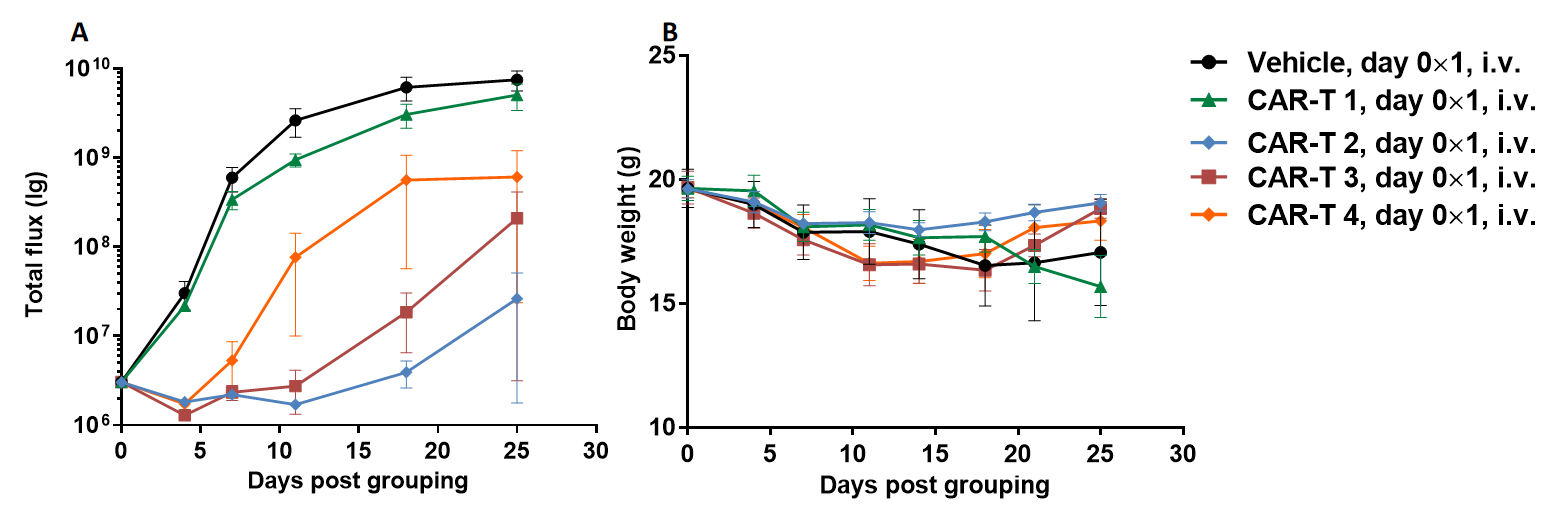
使用B-NDG小鼠建立了Raji淋巴瘤小鼠模型,并验证了抗人CD47抗体的体内药效。B-luc-GFP Raji细胞(5×105)通过尾静脉注射到B-NDG小鼠体内。使用体内成像系统(IVIS)观察肿瘤生长。当肿瘤的荧光强度达到约1×106 p/sec时,将小鼠分为一个对照组和三个治疗组(n=6)。(A) 肿瘤细胞的荧光强度曲线;(B) 体重。结果表明,所有三种抗人CD47抗体均可显著抑制肿瘤生长。B-NDG小鼠是抗人CD47抗体药效验证的有力模型。数据以均值±SEM表示。
严重的异种移植物抗宿主病(xeno-GVHD)会缩短细胞治疗的评估窗口期,影响移植细胞疗法的疗效评估。β2微球蛋白(β2 microglobulin,B2M)是MHC I类分子的组成部分,广泛表达于有核细胞表面,参与机体的自身识别和抗微生物免疫反应。因此,敲除MHC I类分子的β2微球蛋白(β2m)是一种有效降低GVHD发生风险的策略,有助于延长细胞治疗的观察窗口并提高评估效率。
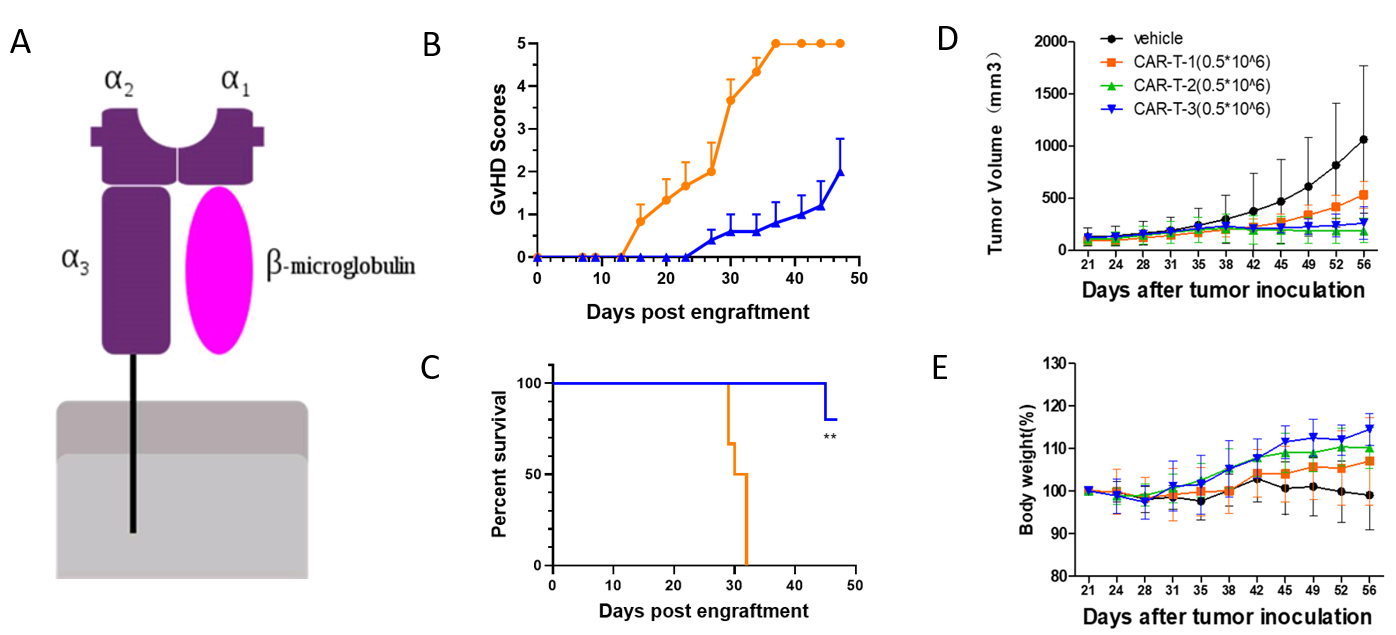
(A) B2M参与MHC I类分子的组成;(B-C) B-NDG B2m KO plus小鼠(蓝线)在植入PBMCs后,相比于B-NDG小鼠(橙线)表现出更低的GVHD评分和更长的生存时间;(D-E) 在B-NDG B2m KO plus小鼠中进行的CAR-T 体内药效研究,展示了肿瘤体积(D)和体重(E)。
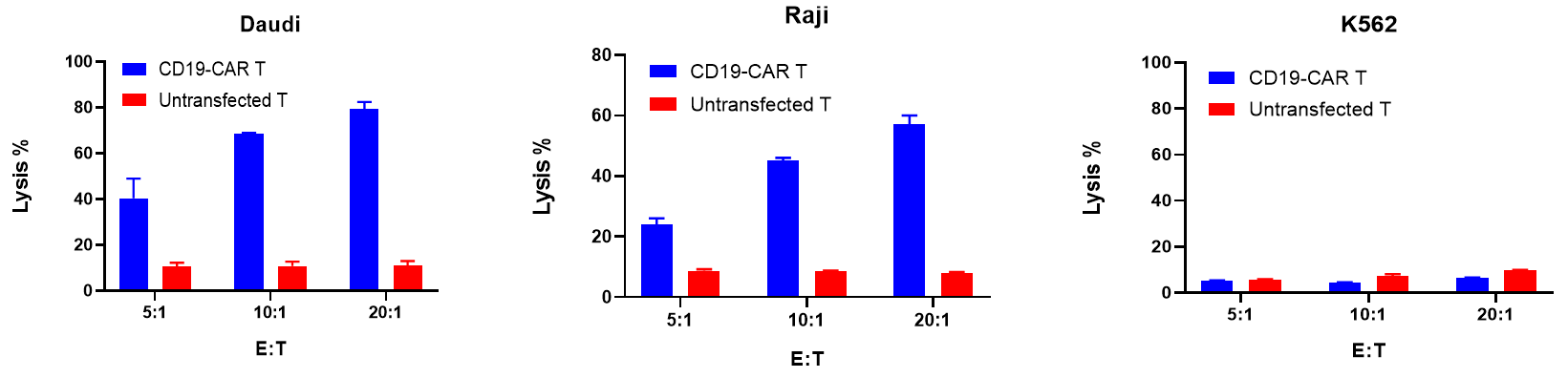
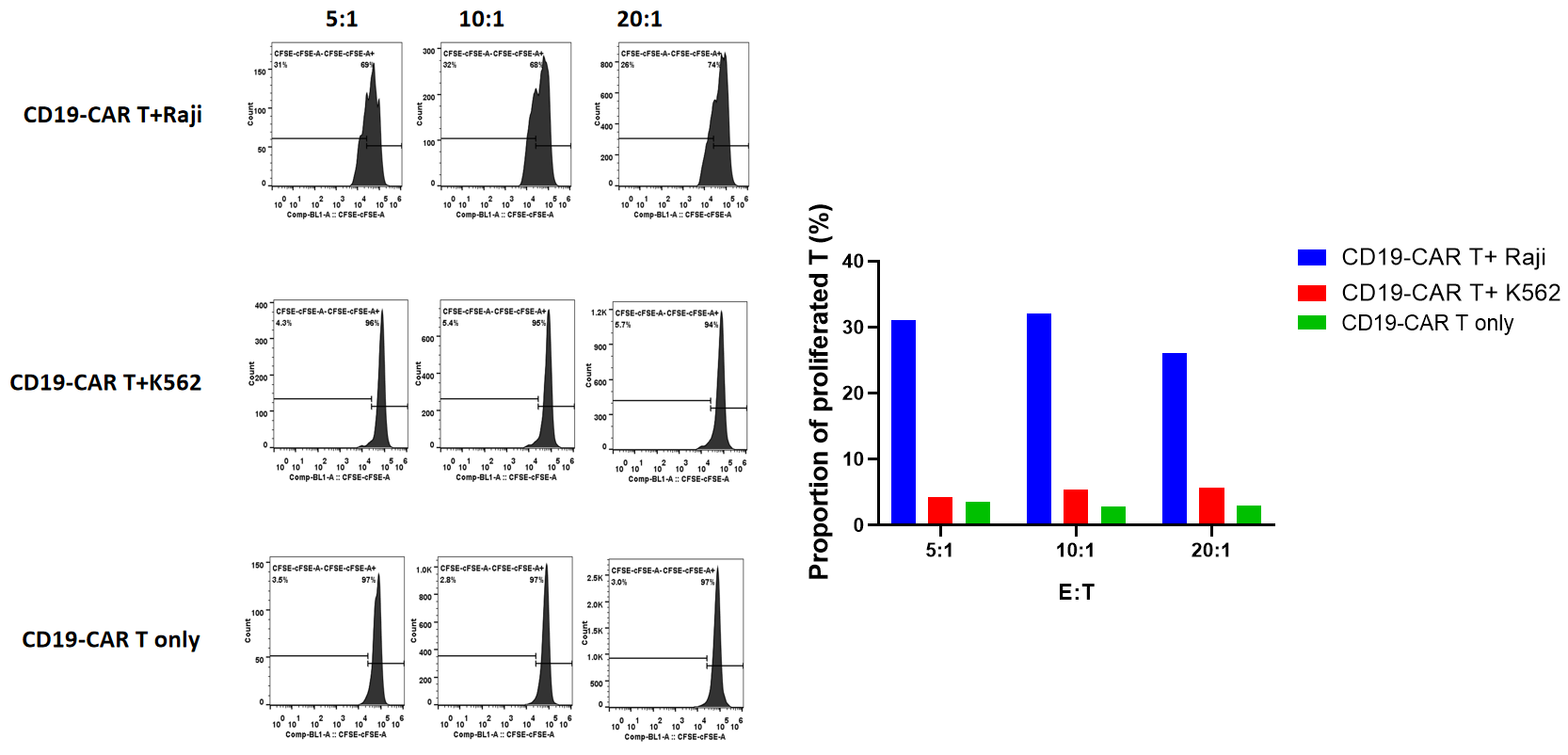
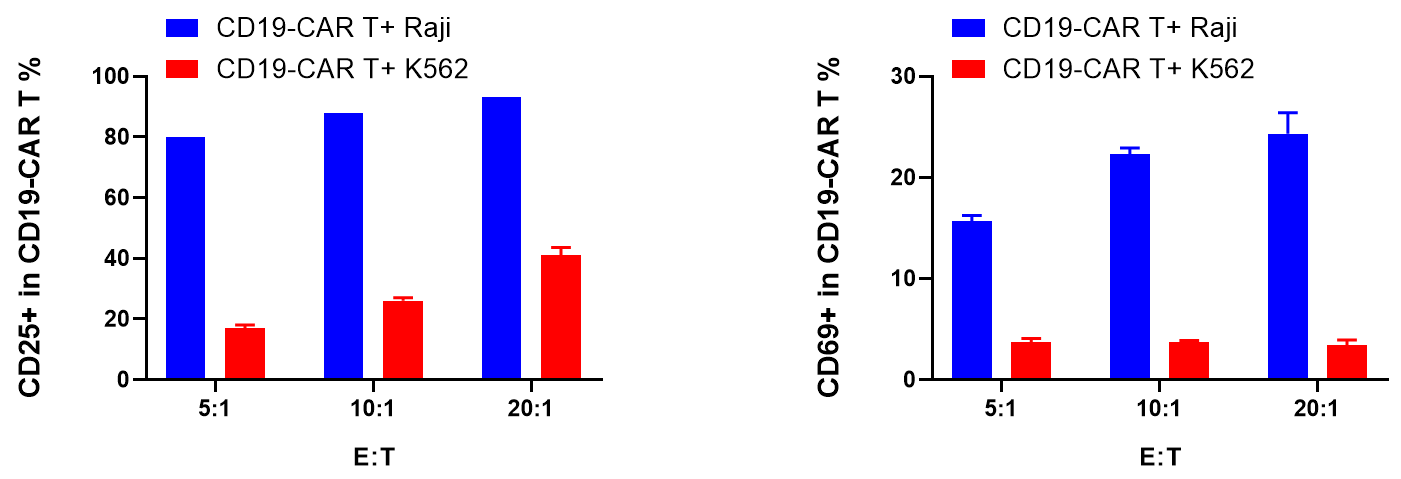
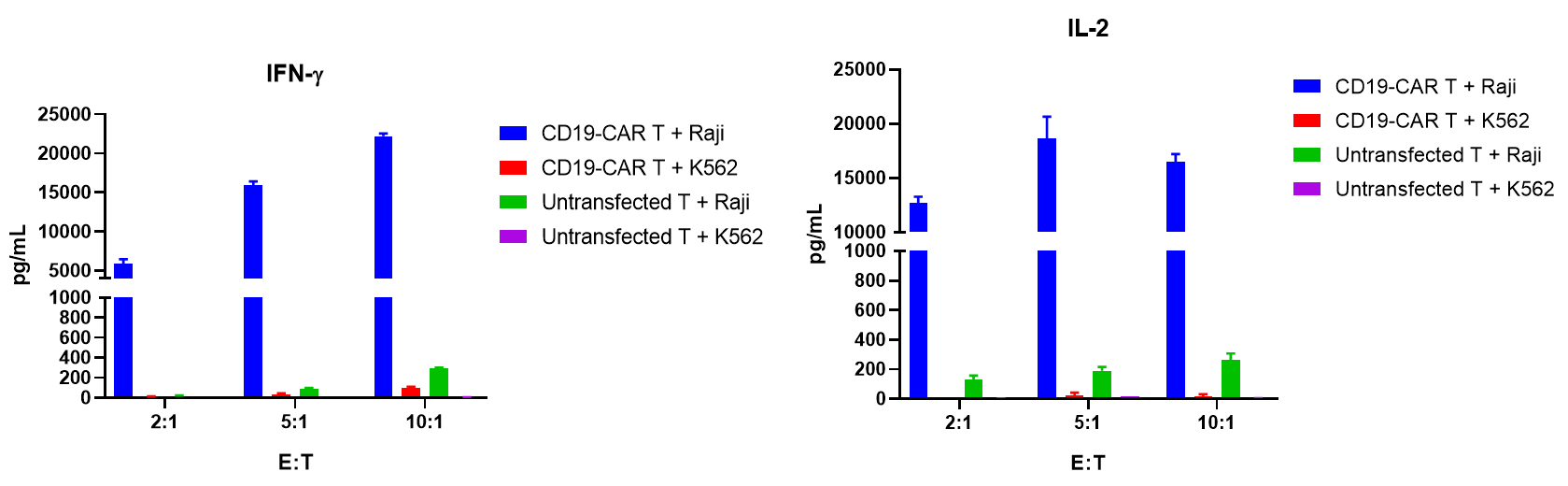
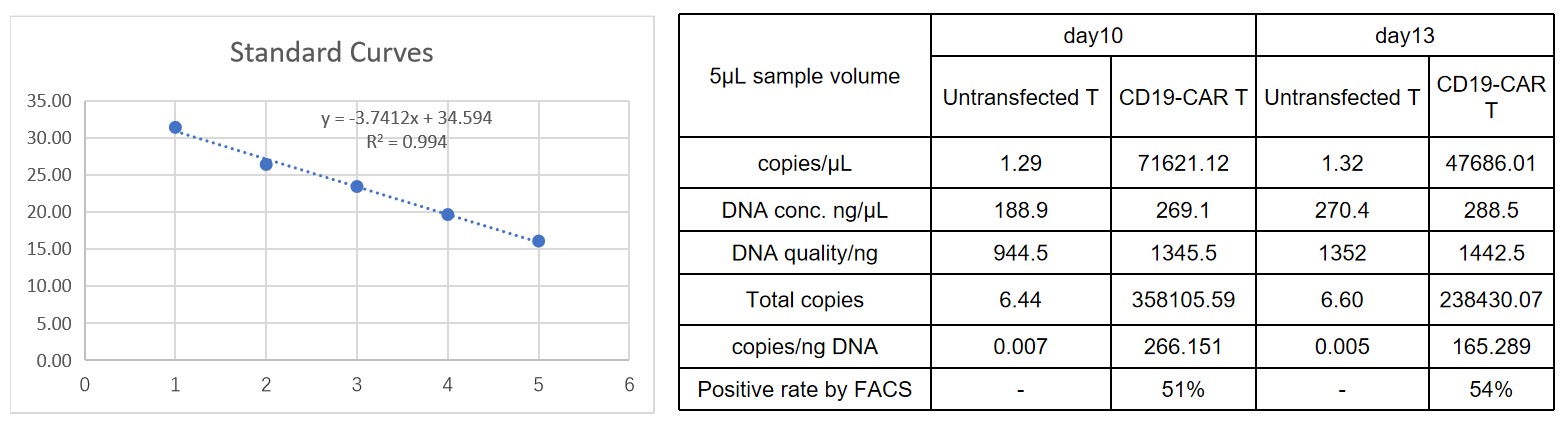
y轴表示Ct值,x轴表示标准拷贝浓度的对数(以10为底)。标准曲线的斜率表示实时PCR扩增效率。当扩增效率为100%时,斜率为-3.32。