在此页面上
小核酸药物,也称为寡核苷酸药物,主要包括反义寡核苷酸(ASOs)、小干扰RNA(siRNAs)、小激活RNA(saRNAs)、微小RNA(miRNAs)、适配体RNA和CpG寡核苷酸等。这些药物通过与核酸(RNA或DNA)相互作用,调控基因表达,从而在遗传或分子水平发挥作用。它们具有高特异性、设计简便、研发周期短、靶点范围广和疗效持久等显著优势。
百奥赛图已开发出一系列专门用于小核酸药物临床前研究的靶点人源化小鼠模型,旨在促进更安全、更有效的核酸治疗药物的研发。
| Efficacy | MOA | Safety |
|
|
|
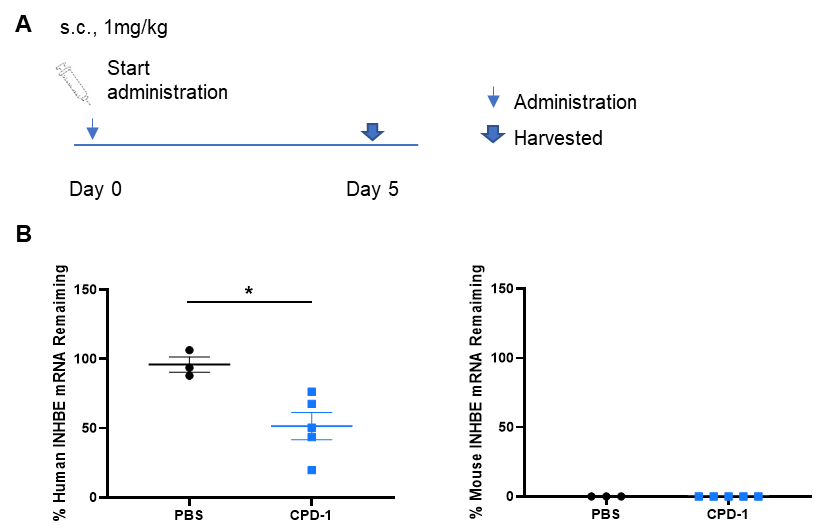
核酸药物对B-hINHBE小鼠中人INHBE的抑制效率。 B-hINHBE小鼠随机分为两组(雄性,9-10周龄)。分别给小鼠单独给予靶向人INHBE核酸药物(由客户提供)和PBS。核酸药物以PBS水溶液的形式给药。小鼠在第5天处死,收集肝组织,采用qPCR检测人类INHBE mRNA的表达水平。(A)实验处理示意图。(B)肝脏中人类INHBE mRNA的表达。CPD-1组中的人类INHBE显著低于对照组。数据以平均值 ± SEM表示。
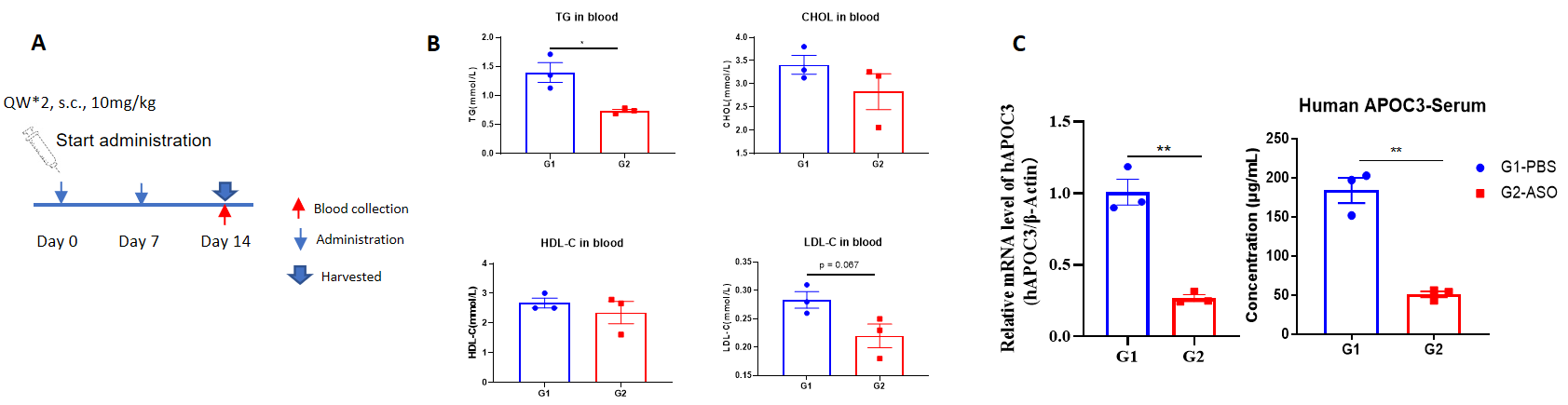
核酸药物对B-hAPOC3小鼠中人APOC3的抑制效率。 B-hAPOC3小鼠随机分为两组(n=3/组,6周龄)。分别给小鼠单独给予靶向人APOC3的核酸药物(根据专利内部合成)和PBS。核酸药物以PBS水溶液的形式给药。所有动物的药物剂量根据体重计算。小鼠在第14天处死,收集肝组织,采用qPCR检测人类APOC3 mRNA的表达水平。(A)实验处理示意图。(B)治疗后B-hAPOC3小鼠的血脂水平。与对照组(G1)相比,治疗组(G2)显示甘油三酯(TG)显著降低。(C)肝脏中人类APOC3 mRNA的表达和血清中的人类APOC3蛋白。治疗组(G2)中的人类APOC3 mRNA显著低于对照组(G1),并且治疗组的抑制率为73.4%,表明B-hAPOC3小鼠为体内评估靶向人APOC3的核酸药物提供了有力的临床前模型。数据以平均值 ± SEM表示。
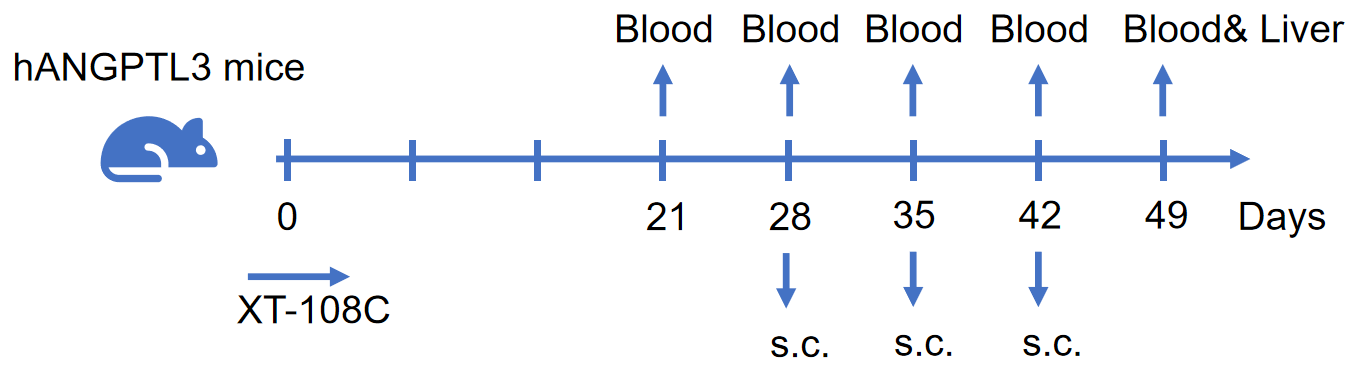
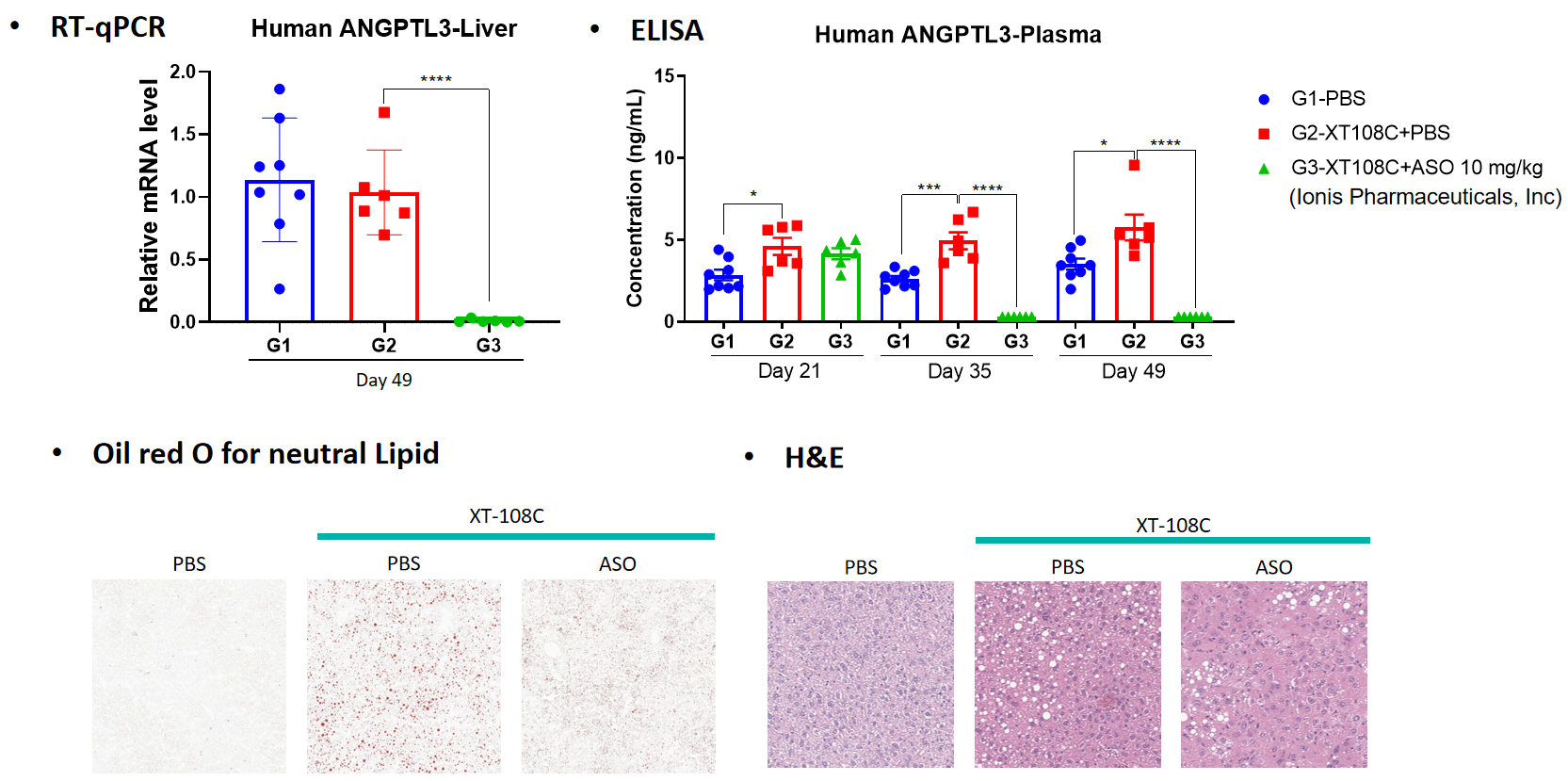
药效学:
病理分析:
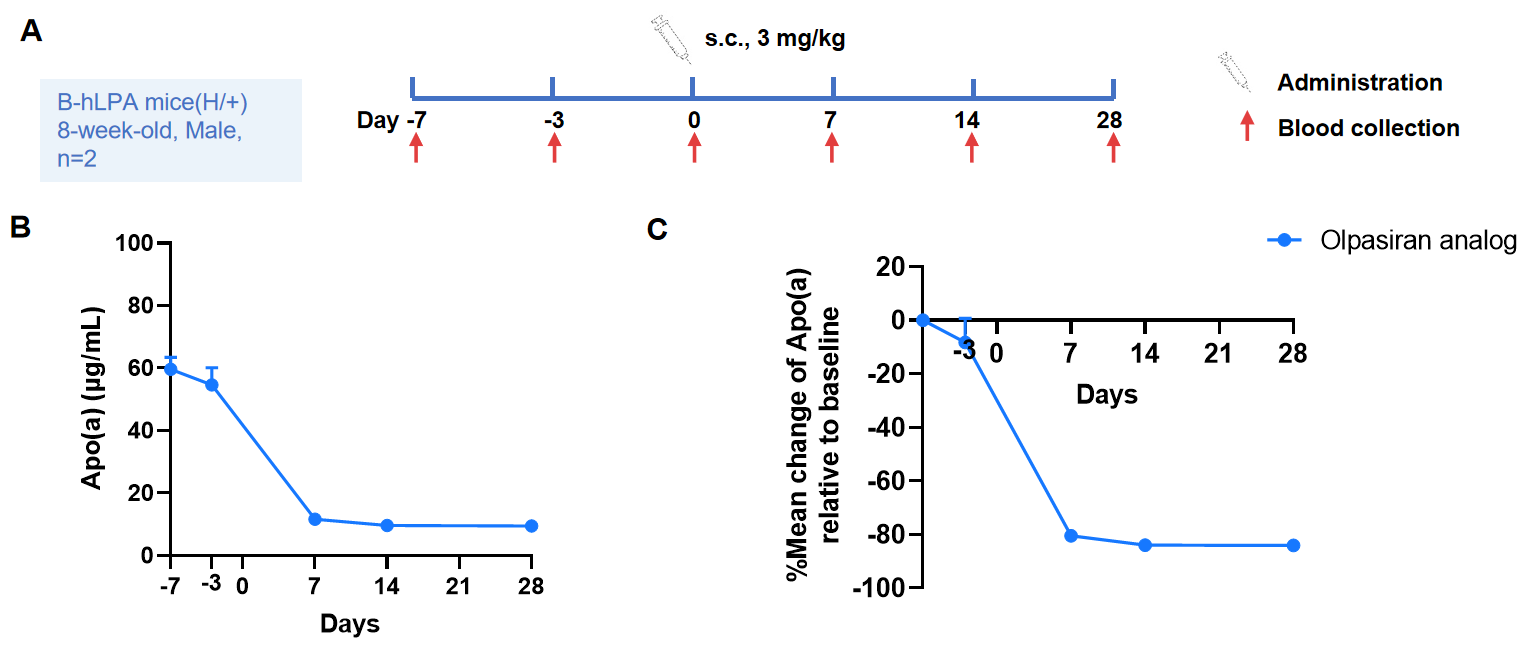
Olpasiran类似物对杂合B-hLPA小鼠血浆apo(a)水平的变化。Olpasiran类似物(由客户提供)是一种靶向脂蛋白(a)的双链小干扰RNA(siRNA),能显著降低血浆Lp(a)浓度。如图所示,Olpasiran类似物在杂合B-hLPA小鼠中降低了Apo(a)浓度(A),在给药后单次给药就能达到超过80%的基线下降(B)。该小鼠可以用于核酸药物的临床前药效研究。
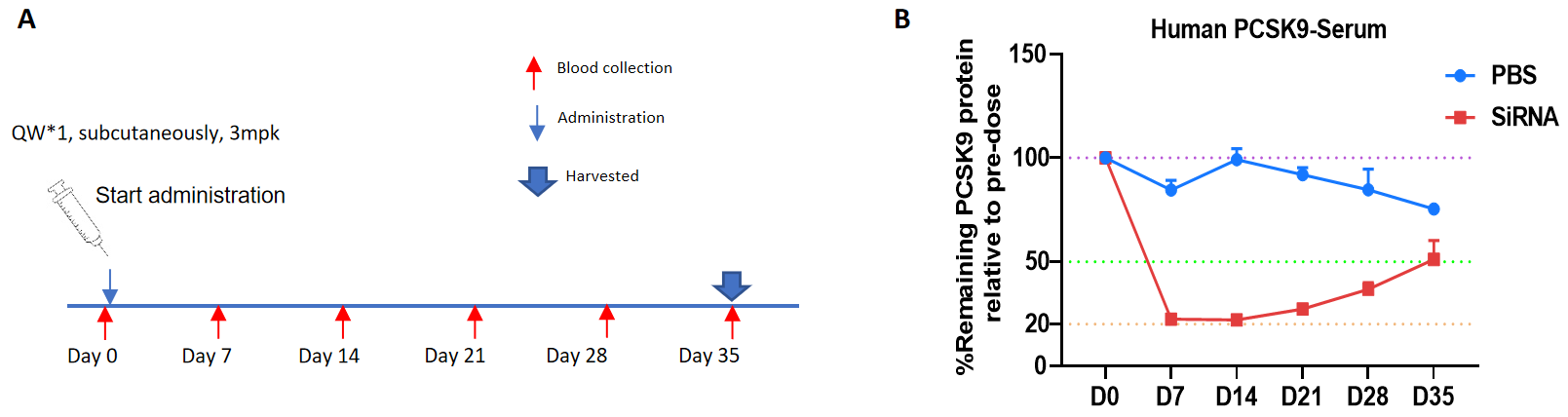
PCSK9靶向小核酸药物在纯合B-hPCSK9小鼠中的抑制效率。B-hPCSK9小鼠被随机分为两组(10周龄,雄性)。靶向人PCSK9小核酸药物Inclisiran(根据专利内部合成)和PBS分别给药。小核酸药物以PBS水溶液的形式给药。小鼠在第35天处死。(A) 实验处理示意图。(B) 在给药后第7、14、21、28和35天,血清中PCSK9蛋白水平的变化,与给药前的水平进行比较。治疗组(G2)的PCSK9水平较对照组(G1)降低,证明B-hPCSK9小鼠为评估人PCSK9靶向小核酸药物的有力的临床前模型。数据以均值±SEM表示。