在此页面上
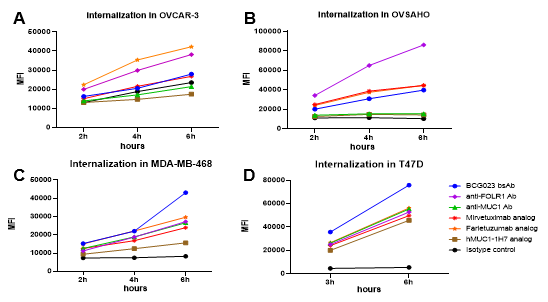
(A-D) BCG023双特异性抗体在四种哺乳动物细胞系中的内吞情况。内吞活性通过流式细胞术(FACS)检测pH敏感染料实现。BCG023在MDA-MB-468 (C)和T47D (D)肿瘤细胞系中表现出优于基准抗体的内吞活性,且较其亲本抗体有明显增强。抗FOLR1抗体在所有细胞系中表现出与基准抗体相当或更强的内吞活性。
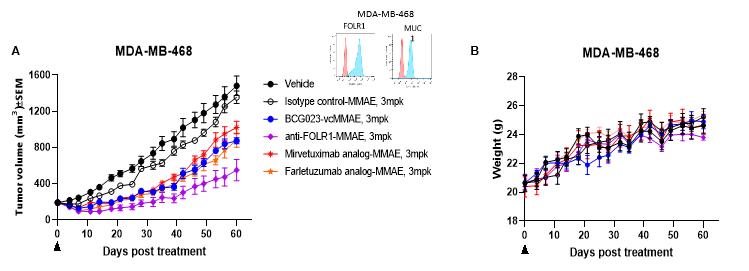
(A) BCG023双特异性抗体偶联药物(bsADC)在三阴性乳腺癌(TNBC)MDA-MB-468异种移植模型中的疗效研究。所有ADC均与vcMMAE偶联,药物抗体比(DAR)约为4。抗FOLR1-MMAE相比两种FOLR1基准ADC表现出更强的抗肿瘤活性,而BCG023-vcMMAE的疗效与FOLR1基准ADC相当。研究期间小鼠体重未见下降。(B)。
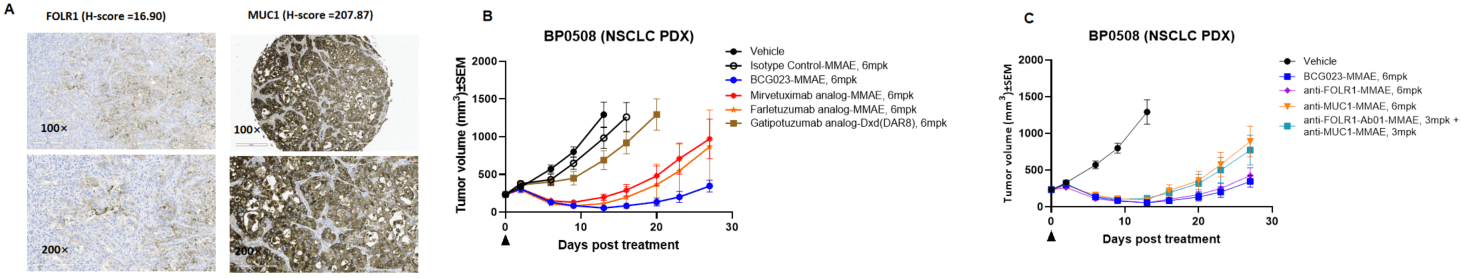
BCG023双特异性抗体偶联药物(bsADC)在低表达FOLR1的非小细胞肺癌(NSCLC)PDX模型中表现出强效的抗肿瘤活性。
(A) PDX模型中FOLR1和MUC1的表达情况。
(B, C) BCG023-vcMMAE的疗效研究。除Gatipotuzumab类似物-Dxd(DAR约为8)外,所有ADC均载有相同的载药(vcMMAE)且药物抗体比(DAR)约为4。BCG023-MMAE在该PDX模型中的疗效优于基准ADC,且较单独的亲本MUC1 ADC或MUC1和FOLR1 ADC联合用药表现出更强的抗肿瘤效果。