您可能也喜欢
自免ADC(用于自身免疫疾病的抗体偶联药物)正在成为行业关注的新方向。2025年以来,多家biotech陆续披露自免ADC临床与临床前数据,释放出清晰信号:ADC的“精准递送”能力,正被用于更温和、更可控的免疫调节场景,为类风湿关节炎、系统性红斑狼疮(SLE)、哮喘、特应性皮炎等疾病提供新的研发路径。
要点速览
1)自免ADC的核心目标从“杀伤”转向“调节”:降低系统性毒性,提升病灶精准性。
2)载荷从细胞毒向激素调节剂、信号通路抑制剂、蛋白降解与核酸递送拓展。
3)靶点更聚焦B细胞、pDC、Th2通路与炎症细胞群,强调“可内吞、可递送”。
4)临床前评估关键在于“物种差异可控”:人源化模型可提升药效与安全性判断可靠性。
自免ADC并非全新概念。早期项目已经验证了“把免疫调节载荷定向送入致病细胞”的可行性。
艾伯维曾推进ABBV-3373(抗TNF抗体偶联糖皮质激素受体调节剂,GRM-ADC)用于类风湿关节炎,并在临床研究中展示了关键逻辑:
通过靶向炎症相关细胞群,将激素样调节剂递送至细胞内释放
期望在维持疗效的同时,降低全身暴露带来的系统性不良反应
后续因管线与战略调整,相关项目推进节奏变化,但其“概念可行性”对行业具有明确启发意义:自免ADC在机制上具备成立基础。
进入2025年,自免ADC思路被系统性放大,企业开始围绕“更安全的递送、更合适的靶点、更可控的载荷”构建管线。公开信息显示:
2025年11月,Lifordi获得赛诺菲旗下风投部门融资,用于推进VISTA ADC LFD-200的CMC与I期研究评估(类风湿关节炎方向)。
国内项目进展更为积极,围绕BDCA2与IL-4Rα等靶点加速布局:
映恩生物:在AIC 2025公布BDCA2免疫调节ADC治疗SLE的I期数据,并推进后续临床。
恒瑞医药:开发吸入式IL-4Rα ADC用于哮喘,强调局部给药与降低入血风险的综合策略。
先声药业:IL-4Rα ADC(SIM0708)披露自免方向临床前研究信息。
博锐生物:BR2060于2026年1月提交临床申请。
肿瘤ADC强调“高杀伤、强细胞毒”。自免ADC则更强调“精准调节、长期可控”:
目标不是广泛清除细胞,而是抑制过度炎症与异常免疫反应
核心评价指标更看重:持久缓解、复发控制、系统性副作用降低、长期用药获益风险比
1)糖皮质激素受体调节剂(GRM):当前主流思路
糖皮质激素是经典抗炎手段,但长期系统性使用会带来骨代谢与内分泌相关风险。自免ADC的关键价值在于:
通过抗体靶向,将GRM更集中递送到致病细胞(如炎性巨噬细胞、活化T细胞等)
期望降低血液系统暴露,从而减少全身副作用
2)小分子通路抑制剂递送:更强的“细胞内精准刹车”
行业也在探索将JAK/STAT抑制剂、PDE4抑制剂等偶联至抗体,实现:
细胞内特定信号通路更精准的阻断
对过度活化免疫细胞实现“定向降噪”式调节
3)分子胶/PROTAC载荷:从“抑制”走向“降解”
以“GLUE-DAC”等概念为代表的策略强调利用泛素-蛋白酶体系统降解致病蛋白:
不依赖活性位点占位,理论上可扩展到更多靶蛋白
具备催化循环特征,可能在较低剂量下维持效应
注:具体技术路线与临床可行性仍需更多数据验证。
4)核酸载荷(如siRNA):从mRNA层面“沉默”炎症驱动因素
通过抗体将siRNA递送至特定细胞(如B细胞、巨噬细胞等),在mRNA层面下调致病基因表达,有望从源头削弱炎症级联反应。该方向对递送效率、稳定性与安全窗要求更高,临床前模型与递送工艺同等关键。
自免ADC靶点更强调两点:
靶点在致病细胞上表达具有相关性
靶点结合后具备内吞特性,便于载荷进入细胞发挥作用
传统抗TNF单抗主要中和可溶性TNFα;而自免ADC思路之一,是靶向表达于活化免疫细胞表面的跨膜型TNFα(tmTNF),通过内吞递送GRM等载荷,在细胞内抑制炎性因子产生源头。
SLE中,浆细胞样树突细胞(pDC)是I型干扰素的重要来源。BDCA2是pDC表面特异性受体,且结合后可内吞。利用该特性可将免疫调节载荷递送至pDC,从而抑制TLR7/9相关的促炎因子释放(以企业公开研究信息为参考)。
针对Th2型炎症,阻断IL-4/IL-13信号是关键策略。IL-4Rα ADC的差异化思路在于:
除受体阻断外,借助内吞递送载荷,延长或增强局部免疫调节
结合给药方式创新(如吸入给药),进一步降低系统暴露风险
提示:IL-4Rα存在物种差异,临床前模型选择对结果解释影响显著。
B细胞相关靶点(CD19/CD20/BCMA/CD79b)
B细胞清除是多种自免疾病的重要治疗路径。通过ADC实现对自身抗体相关B细胞群更深入的调控,理论上可用于难治性SLE等场景的“免疫重置”探索。具体策略需结合安全性窗口、感染风险监测与长期随访数据综合评估。
概念成立只是起点。自免ADC评价需要同时回答三类问题:
递送是否真正到达“致病细胞/病灶组织”?
免疫调节是否足够强且可持续?
系统暴露与安全窗是否优于传统系统给药?
许多自免靶点(如IL-4Rα)存在显著种属差异。普通野生型小鼠可能无法准确反映:
人源抗体与人源靶点的结合与内吞
载荷在真实靶点背景下的药效强度与安全性边界
因此,人源化模型在自免ADC临床前阶段具有更高解释力。
百奥赛图开发了系列自免相关靶点的人源化小鼠模型,包括B-hIL4/hIL4RA小鼠等,可用于:
抗体药物与自免ADC药效评价
安全性与系统暴露相关风险评估(需结合研究设计)
深入到细胞内信号环节:评估如STAT6等下游关键节点药物(包括PROTAC类策略)对信号传导与炎症基因转录的体内影响
从“受体阻断”到“信号沉默”,实现同一模型支持多类候选药物验证,提高项目筛选效率与决策质量。
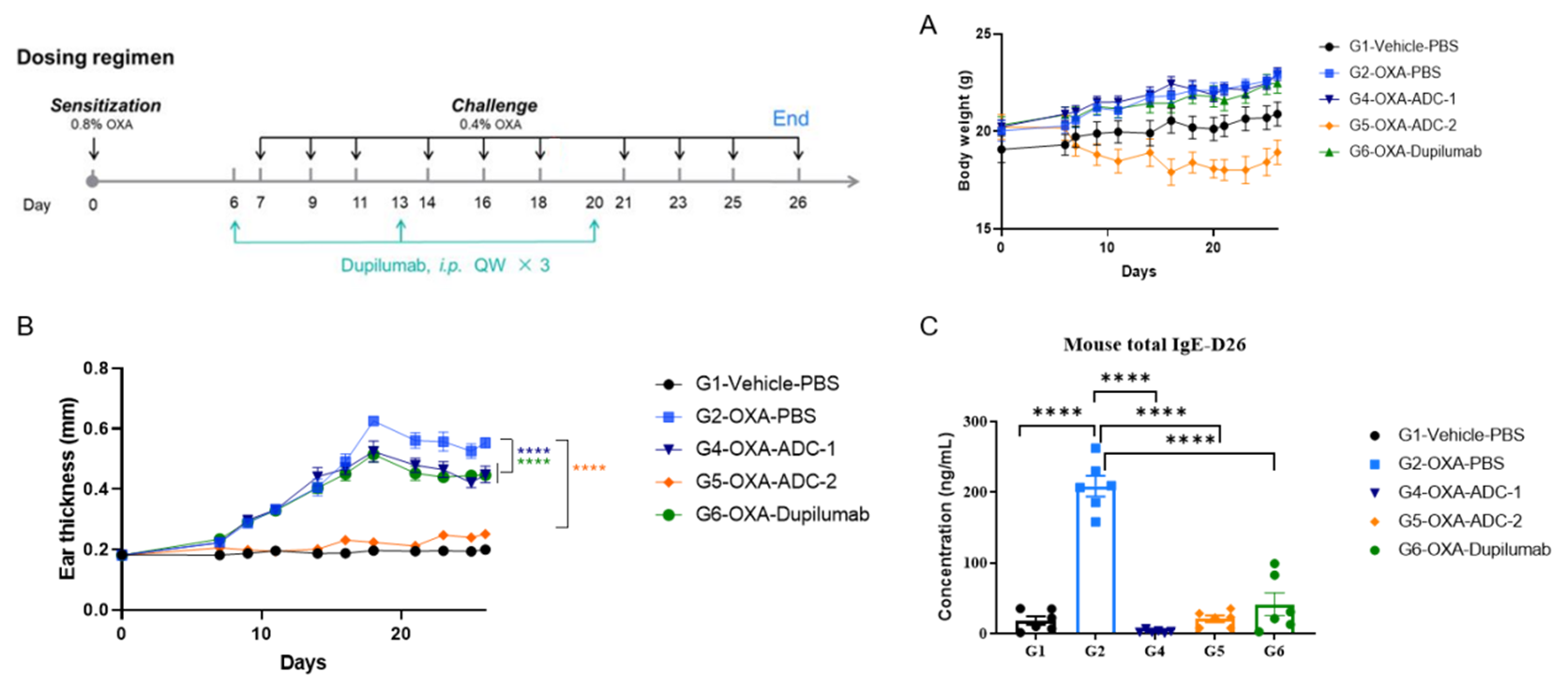
抗人IL4RA抗体及ADC药物在B-hIL4/hIL4RA小鼠中的药效评估。 各组小鼠经腹腔注射给予抗hIL4RA抗体和ADC药物(药物由客户提供,每组n=6)。 (A) 治疗期间的体重变化。 (B) 各组耳部厚度的统计分析。 (C) 血清中总IgE水平。结果显示,与未治疗组(G2,模型组)相比,接受抗IL4RA抗体和ADC药物治疗的小鼠组耳部厚度显著降低。 在实验终点采集血清,并通过ELISA分析IgE水平。结果显示,接受抗人IL4RA抗体和ADC药物治疗的小鼠,其总IgE水平和耳厚明显低于未治疗组小鼠。 数值以Mean±SEM表示。显著性通过双因素方差分析(two-way ANOVA)确定。 *P < 0.05, **P <0.01, ***P < 0.001, ****P < 0.0001。(客户合作数据)
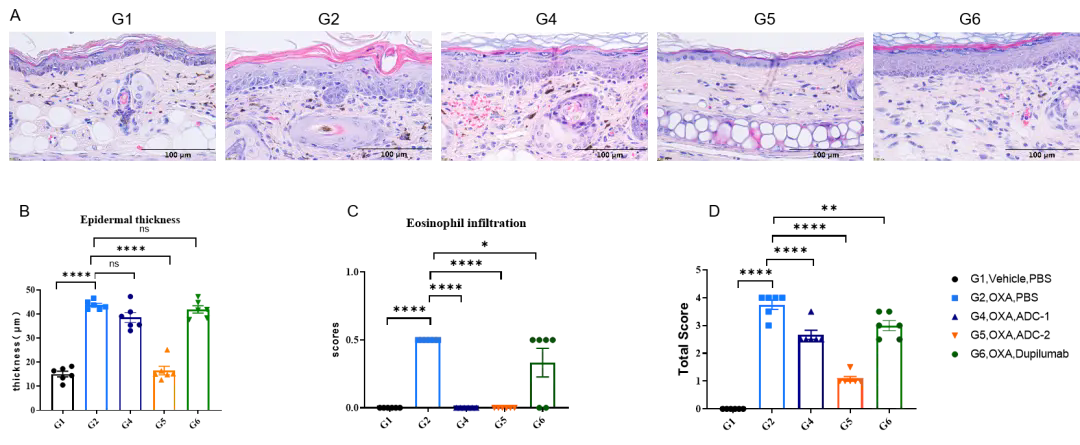
耳部病理评分及表皮厚度。在实验终点采集耳部组织并进行H&E染色分析。结果显示,与未治疗组(G2)相比,接受ADC药物(由客户提供)治疗的小鼠组,其耳部皮肤表皮厚度和病理评分显著降低。数值以Mean±SEM表示。显著性通过双因素方差分析(two-way ANOVA)确定。 *P < 0.05, **P < 0.01, ***P < 0.001,****P < 0.0001(客户合作数据)
B-hIL4/hIL4RA小鼠的应用潜力不止于疗效曲线:
传统抗体与自免ADC:可并行对比递送与持续性效应差异
安全性评价:结合给药频次、剂量探索与组织暴露数据,辅助确定候选分子窗口
机制验证:支持对Th2通路下游(如STAT6)调控策略的体内验证,为PROTAC等新型载荷/策略提供更贴近临床的评估环境
结论是:在靶点存在物种差异的自免方向,模型选择本身就是“研发效率”的一部分。
2025年以来,自免ADC热度快速上升,背后是明确的技术路径变化:
载荷更温和、更精准、更可组合
靶点更强调内吞与细胞选择性
评估更依赖人源化模型与机制证据链
当“精准递送”从肿瘤扩展到免疫稳态调控,自免ADC有望成为连接抗体工程、递送技术与免疫生物学的新型平台方向。项目能否走得更远,最终仍取决于:可重复的疗效数据、可接受的长期安全性与清晰的临床获益人群定位。
参考资料:
1、Zhou M, et al.The next frontier in antibody-drug conjugates:
challenges and opportunities in cancer and autoimmune therapy. Cancer Drug Resist. 2025 Jul 3;8:34.
2、Buttgereit F, et al. Efficacy and Safety of ABBV-3373, a NovelAnti-Tumor Necrosis Factor Glucocorticoid Receptor Modulator Antibody-Drug Conjugate, in Adults with Moderate-to-Severe Rheumatoid Arthritis Despite Methotrexate Therapy: A Randomized, Double-Blind, Active-Controlled Proof-of-Concept Phase IIa Trial. Arthritis Rheumatol. 2023 Jun;75(6):879-889.
3、Pal LB, et al. An Overview of the Development and Preclinical Evaluation of Antibody-Drug Conjugates for Non-Oncological Applications. Pharmaceutics. 2023 Jun 24;15(7):1807.