您可能也喜欢
小鼠体外受精(In Vitro Fertilization,IVF)技术在生殖生物学研究与基因工程动物模型制备中应用广泛。与自然交配相比,小鼠 IVF 可在短时间内获得更多同步胚胎,提升珍贵品系繁殖效率,并支持冷冻精子保种与后续胚胎操作。
小鼠 IVF 的主要优势包括:
获得大量同步发育胚胎,便于统一实验窗口
提高珍贵品系与低繁殖力品系的繁殖效率
支持冻精复苏与品系保种,便于资源管理
便于开展胚胎显微操作,如胚胎移植与基因编辑衔接
小鼠 IVF 通过体外模拟体内受精环境,使精子在培养体系中获能并与卵母细胞结合,启动受精与早期胚胎发育。
核心步骤包括:
精子获能
卵母细胞采集
精卵共培养
胚胎发育观察与筛选
成功关键在于培养基成分、温度、气体环境与时间节点的稳定控制。
雄鼠:8–12 周龄,性成熟且健康
可先与雌鼠合笼评估交配情况
IVF 前一周建议单独饲养,用于测试生育能力
雌鼠:可群养
建议选择 4–5 周龄或 8–10 周龄进行超排卵
该周龄段排卵数量与质量更易稳定
HTF 体外受精培养液
可选用百奥赛图自研试剂
与自研 PM 联合使用时,文中描述受精率可达 80% 以上(具体效果受鼠系与操作影响)
PM 精子获能液(可选百奥赛图自研试剂)
矿物油(胚胎培养级)
M2 与 KSOM 培养基(胚胎操作与培养)
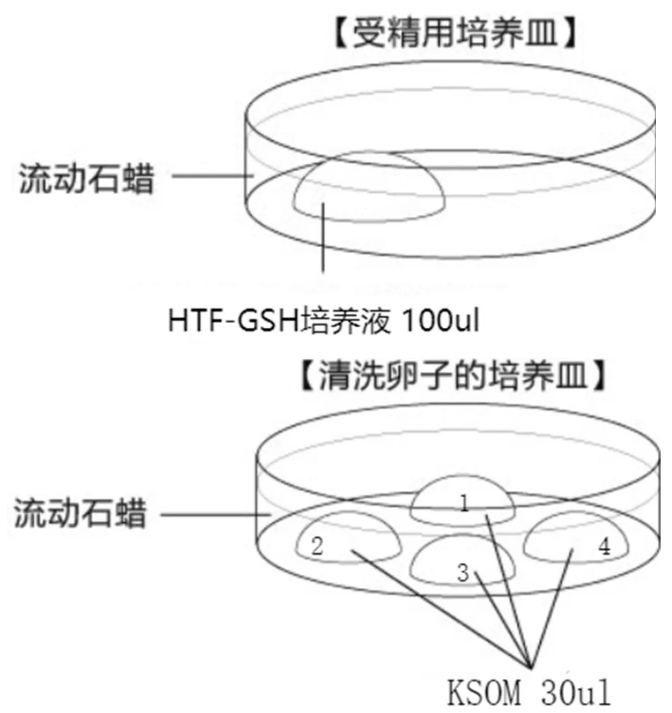
HTF 微滴:100 μL/滴
单滴对应 2–3 只雌鼠排卵量
特殊课题或冻精复苏可使用 HTF-GSH(含谷胱甘肽)
采卵前 30 分钟完成制备,在 CO₂ 培养箱平衡 ≥30 分钟,也可过夜平衡
PM 微滴:100–200 μL/滴
按雌鼠数量增减
KSOM 微滴:采胚胎前 30 分钟完成制备
在 CO₂ 培养箱平衡 ≥30 分钟,也可过夜平衡
体视显微镜
CO₂ 培养箱(37℃,5% CO₂)
恒温台
冷光源
胚胎培养皿、口吸管等
实验室温度:约 25℃
超净工作台操作
所有器械严格灭菌处理
建议下午 4 点左右对雌鼠进行腹腔注射。不同背景鼠系的推荐方案如下:
C57BL/6、BALB/c 等背景鼠:
第一次注射 FSH(促卵泡素)
间隔 72 小时后第二次注射 HCG(人绒毛膜促性腺激素)
NDG 背景免疫缺陷鼠:
第一次注射 PMSG(孕马血清促性腺激素)
间隔 48 小时后第二次注射 HCG(人绒毛膜促性腺激素)
文中说明:以上激素可由百奥赛图试剂生产部供应。
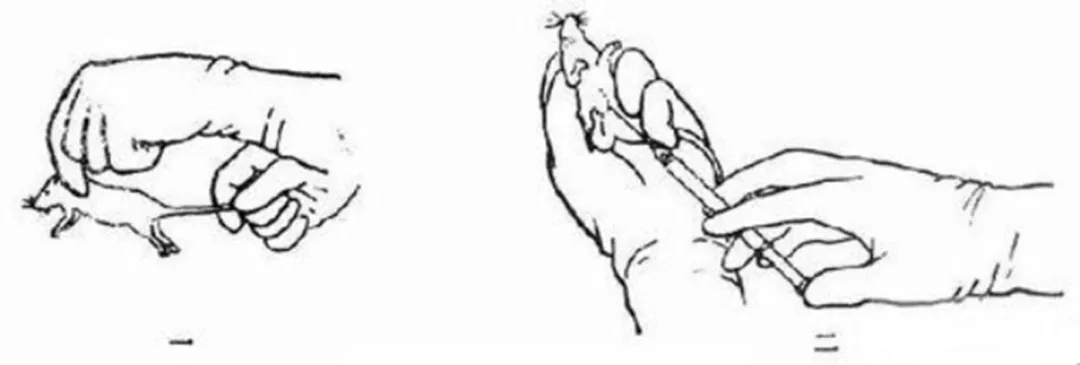
HCG 注射后 13–15 小时处死雌鼠
取出输卵管,在体视显微镜下定位壶腹部
用细针轻撕膨大部,释放卵丘-卵母细胞复合体(COCs)至 HTF 微滴
将培养皿置于培养箱备用
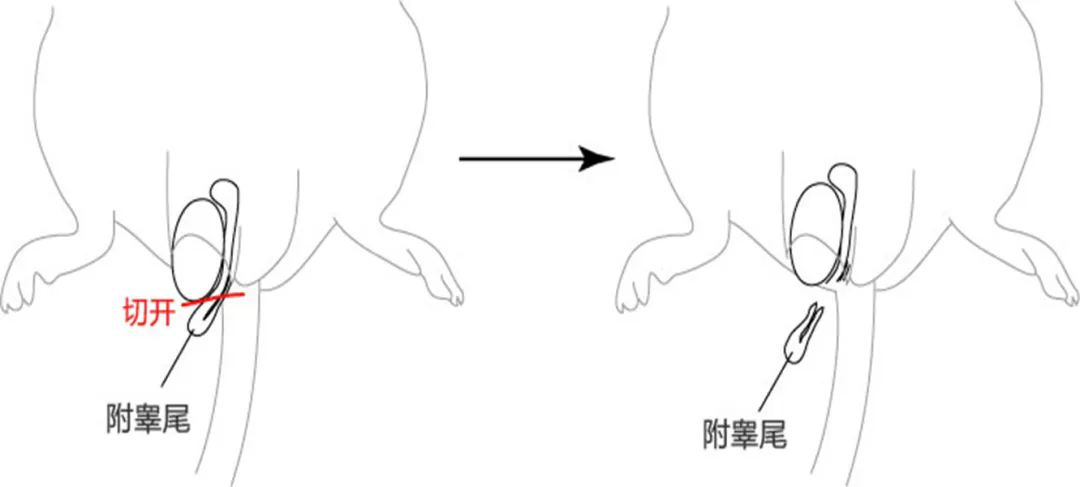
处死雄鼠,或对活体雄鼠麻醉后取单侧附睾尾
剔除血丝后剪开附睾尾
轻挤压使精液流出,置于 PM 微滴中
将精子微滴置于培养箱孵育 1 小时,使精子获能
可观察精子活力
获能良好时可见较活跃的运动表现
用移液器吸取上层活跃精子
释放到 HTF 微滴中用于受精
将培养皿放回培养箱
精卵共培养 4–6 小时完成受精过程
受精后约 24 小时(次日上午)
在体视显微镜下挑选培养皿中的 2-cell 胚胎
用口吸管转移至 KSOM 微滴
覆盖矿物油继续培养
用于后续胚胎移植
小鼠输卵管移植是将胚胎或配子通过外科手术方式移植到受体雌鼠输卵管内,使其在体内继续完成后续发育的核心生殖技术。与子宫移植相比,输卵管移植主要适用于早期胚胎(原核期至桑椹胚阶段),用于衔接 IVF、基因编辑等体外操作与体内发育过程。
受体鼠:ICR 雌鼠
推荐周龄:8–10 周龄
推荐体重:28–35 g
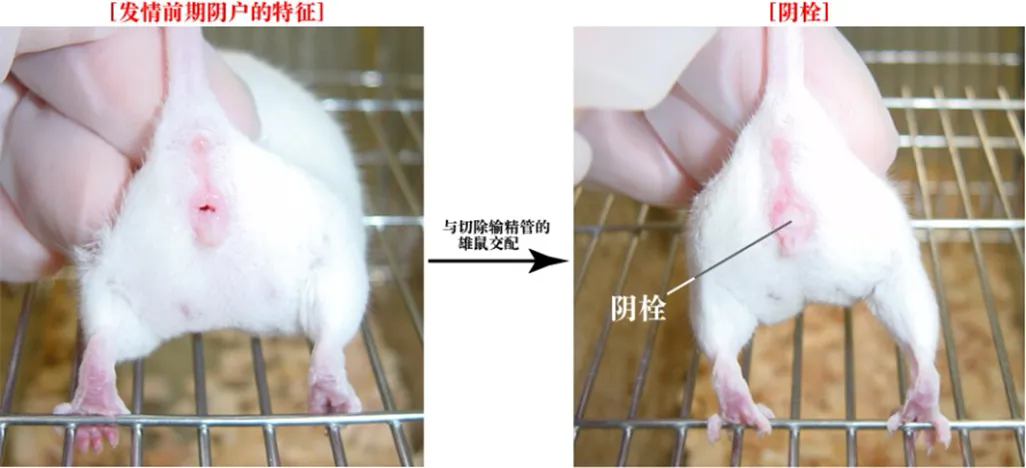
胚胎移植前 1–3 天,将受体雌鼠与结扎雄鼠合笼自然交配。移植当天检查阴道口出现阴栓的 ICR 雌鼠,确认形成假孕环境后单独挑出待用。
适用胚胎时期:
受精卵与 2-cell 胚胎为主
4–8-cell 胚胎亦可
胚胎来源包括:
体外受精实验
胚胎复苏实验
自然合笼后冲取输卵管获得胚胎
腹腔注射麻醉剂:舒泰50 + 盐酸赛拉嗪
皮下注射止痛剂:卡洛芬
麻醉深度:脚趾捏夹无反应
术前处理:背部剃毛(约 2×3 cm),酒精消毒皮肤
建议两人配合操作:主操作人负责胚胎移植,辅助人员负责动物外科操作。
步骤如下:
最后肋骨后方 1 cm、脊柱旁开 0.5 cm 处提起皮肤
剪开约 1 cm 皮肤切口
钝性分离肌肉层
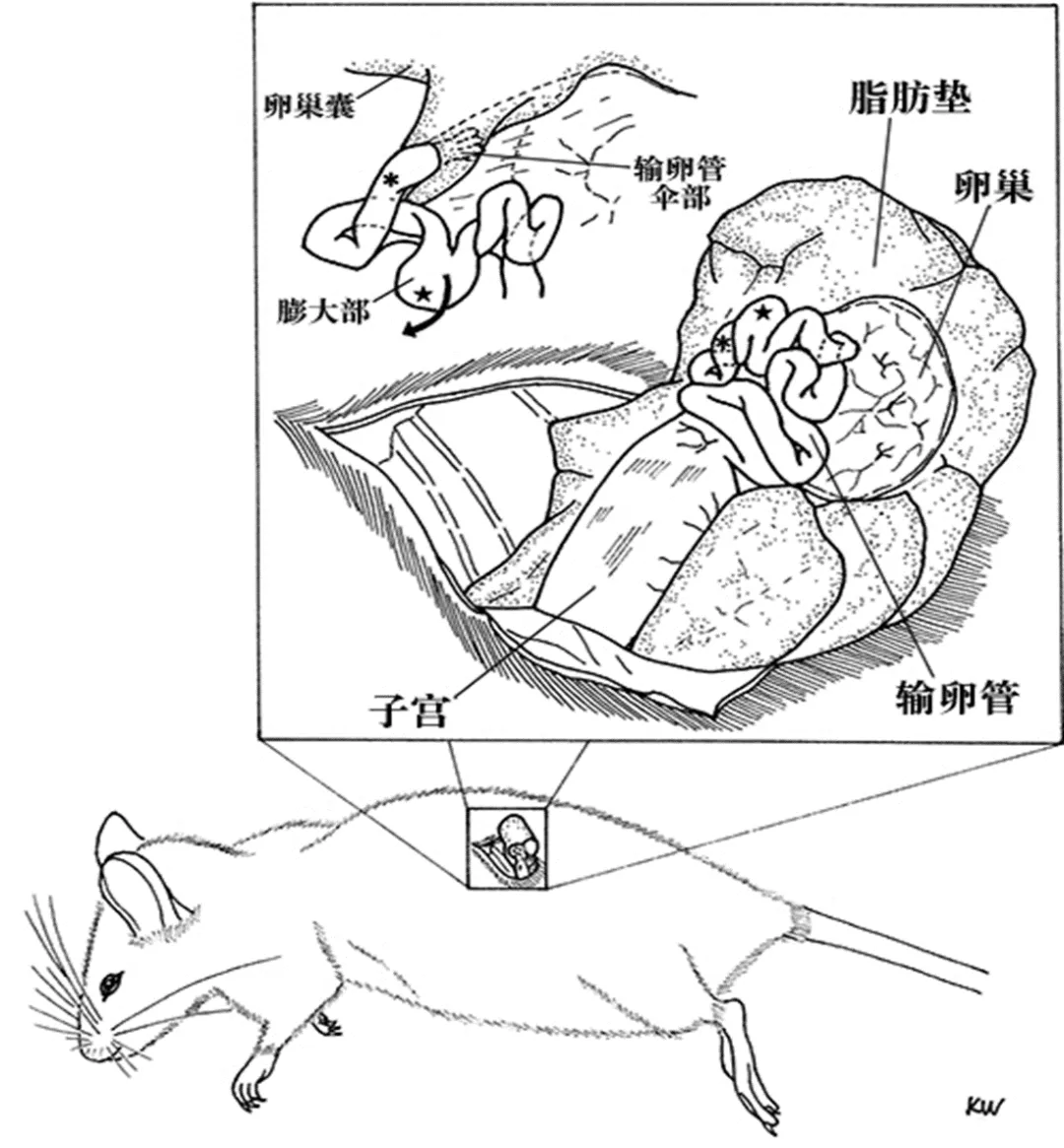
拉出脂肪垫,暴露卵巢与输卵管
用微血管夹固定脂肪垫于背部皮肤
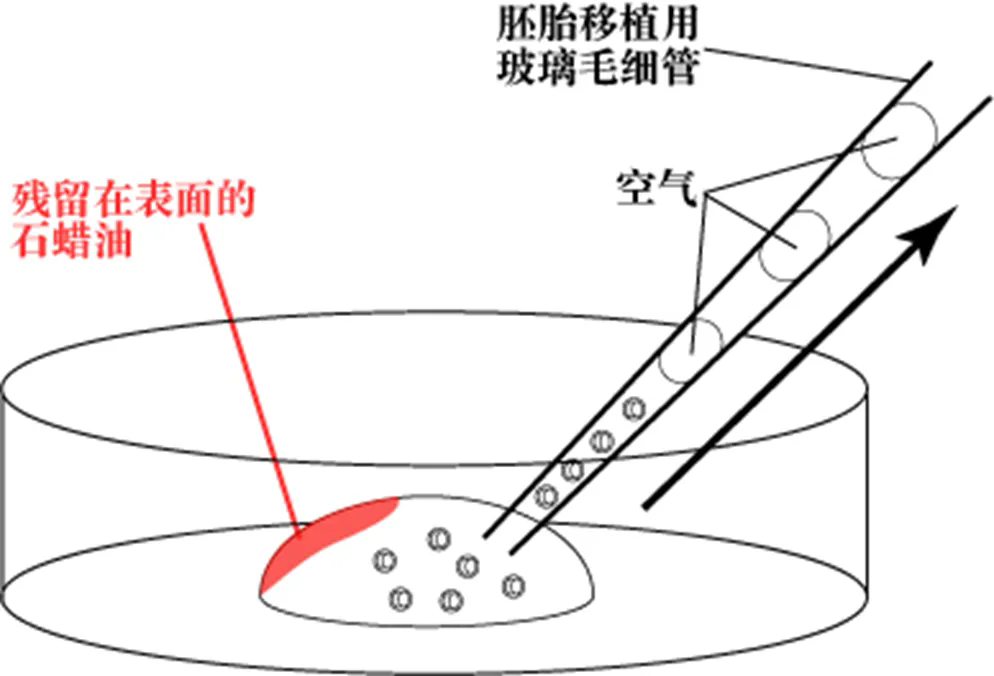
在体视显微镜下用口吸管-移植针装置装载胚胎,装载顺序为:
培养基 → 气泡 → 胚胎 → 气泡 → 培养基
单侧输卵管推荐胚胎数:8–12 枚
单次移植针吸取胚胎数:约 6 枚
具体可根据操作者速度调整
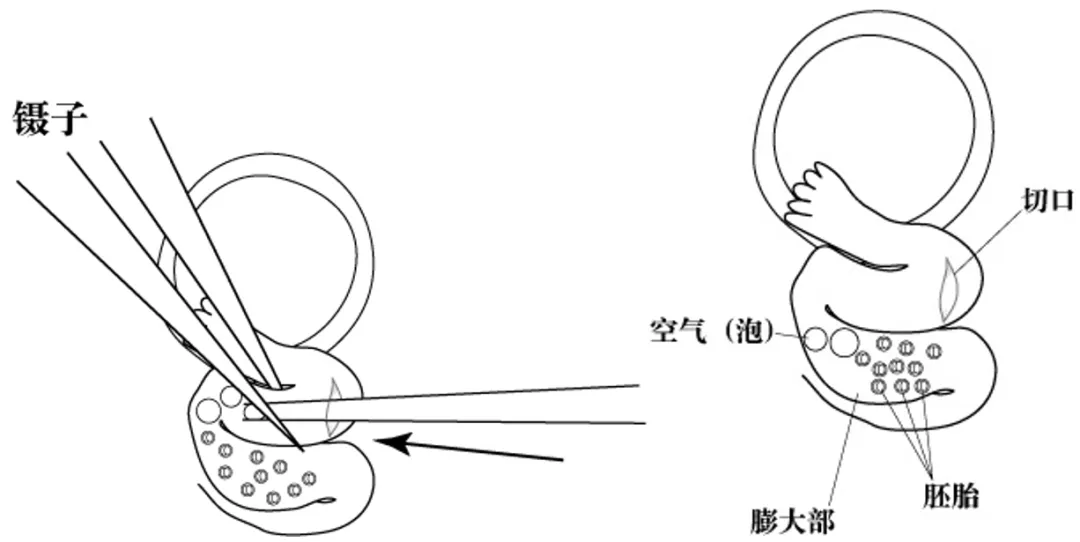
显微镊夹持输卵管膨大部
伞部为常用进针位置,也可选择伞部向上、距膨大部 2 个拐弯处
用 1 mL 注射器针尖在进针点扎开小口
将移植管尖端从开口进入并探入膨大部
缓慢吹出胚胎,观察气泡进入输卵管
短暂停留后撤出移植管
检查移植管尖端,确认胚胎已全部吹出
松开血管夹
将生殖器官放回腹腔
缝合肌肉层与皮肤
加热垫复温,维持 37℃
观察呼吸与心跳,直至恢复自主活动
单笼饲养并提供饲料与饮水
前 5 天每日观察活动与饮食
每日观察伤口愈合情况
移植约 14 天显怀
移植约 19 天分娩
小鼠 IVF 技术是生殖生物学与遗传学研究的重要工具。随着技术发展,IVF 将与基因编辑、干细胞等技术持续融合,为生物医学研究提供更高效的模型构建路径。
参考文献
《小鼠胚胎操作实验手册》(原著第三版)
图片来源
网站《小鼠生殖工程学技术》(jinpanbio.com)