您可能也喜欢
慢性疼痛是重要公共卫生问题。疼痛并非单一症状,而是复杂神经调控过程[1]。在神经损伤或组织炎症后,电压门控钠离子通道(VGSCs)会放大并维持异常放电。其中,Nav1.8(SCN10A)被视为慢性疼痛的关键调控节点,也是非阿片类镇痛研发的重要方向。
VGSCs决定动作电位的产生与传播。外周伤害感受器被激活后,钠通道电流变化可提高神经元兴奋性,从而增加疼痛信号输入[1]。在众多亚型中,Nav1.8主要分布于外周感觉神经元,参与高频放电与疼痛维持,被认为更贴近“外周疼痛信号通路”。
研究显示,Nav1.8在疼痛不同阶段呈动态变化,并与Nav1.7共同参与信号放大[2]。
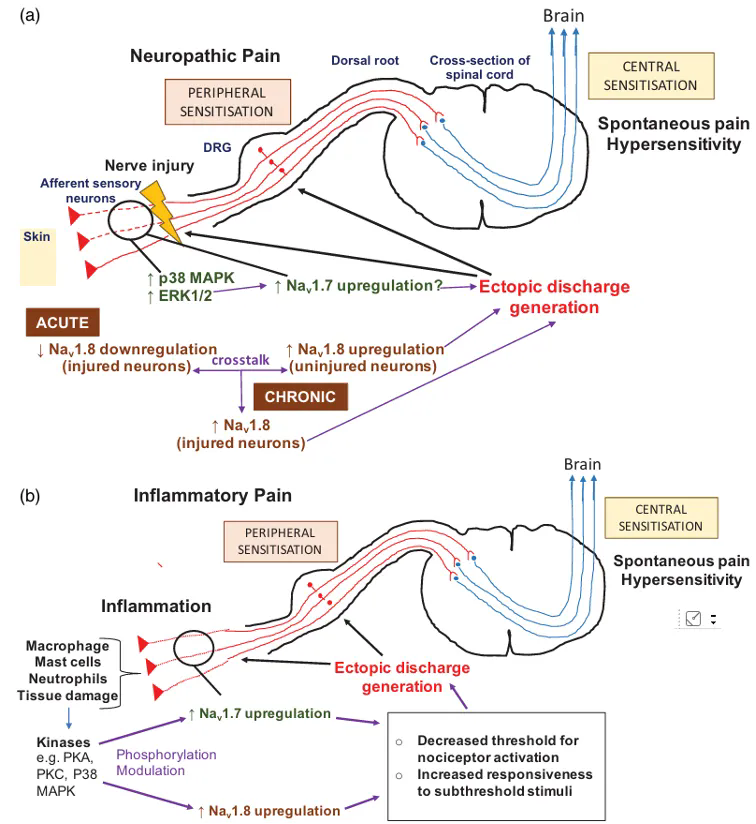
Nav1.7与Nav1.8在神经病理性疼痛与炎症性疼痛中的作用机制示意图
神经损伤初期:受损神经元内Nav1.8表达可下调
邻近未受损神经元:Nav1.8表达上调
结果:未受损神经元自发放电增加,诱发异常疼痛信号[2]
受损与完整神经元出现“串扰”(crosstalk)
串扰促进受损神经元内Nav1.8再上调
结果:异位放电(ectopic discharge)增强并持续
表现:自发性疼痛与痛觉过敏长期存在[2]
炎性细胞与炎症介质会激活多种激酶信号通路。激酶可通过磷酸化调控Nav1.7/Nav1.8,并促进其在伤害感受器中的表达上调,从而增加异常动作电位并放大疼痛信号[2]。
近两年,Nav1.8相关项目持续推进,并出现获批产品与并购交易。以下信息来自公开披露与监管公告。
2025-01-30:FDA批准Journavx(suzetrigine,VX-548)用于成人中重度急性疼痛。
2025-05-27:Eli Lilly宣布收购SiteOne Therapeutics,交易金额最高可达10亿美元,并获得其Nav1.8抑制剂项目STC-004。
除跨国药企外,多家Biotech也在加速推进差异化布局:
对高选择性Nav1.8抑制剂而言,跨物种通道结构差异可能影响结合位点与药效读出。仅依赖啮齿类同源通道,可能增加临床外推不确定性。
因此,在人源化背景下构建具备功能表达的Nav1.8(SCN10A)模型,可用于:
更贴近人源靶点的体内药效评估
剂量-效应与起效时间的比较
与炎症/术后等不同疼痛模型结合,提升项目决策效率
百奥赛图提供基因人源化模型与疼痛表型测试体系,可用于围绕Nav1.8(SCN10A)的靶点验证与候选药筛选。


在野生型SD大鼠和B-Tg(hSCN10A)、Scn10a KO大鼠中,足底切口明显降低了机械痛阈值。在野生型SD大鼠中,60 mpk的VX-548明显减轻了术后疼痛,镇痛效果持续2小时,而10 mpk的VX-548则没有效果。在B-Tg(hSCN10A)、Scn10a KO大鼠中,VX-548在10 mpk下显著缓解术后疼痛,镇痛作用持续时间长达2小时。B-Tg(hSCN10A)、Scn10a KO大鼠为体内评价靶向人Scn10a镇痛药物的疗效提供了强有力的临床前模型。(A)分组和治疗。(B)术后疼痛建模示意图。(C) VX-548的镇痛作用。*P < 0.05, **P < 0.01, ***P < 0.001.
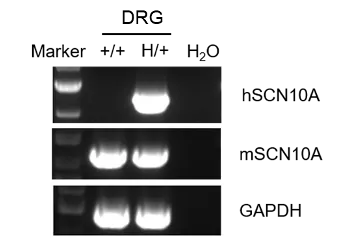
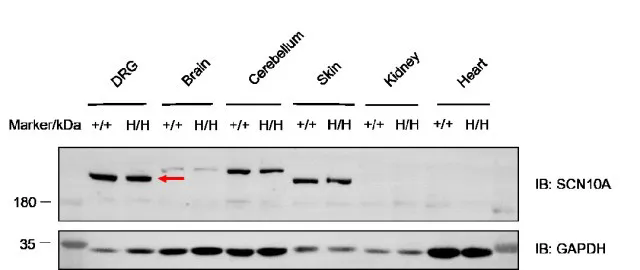
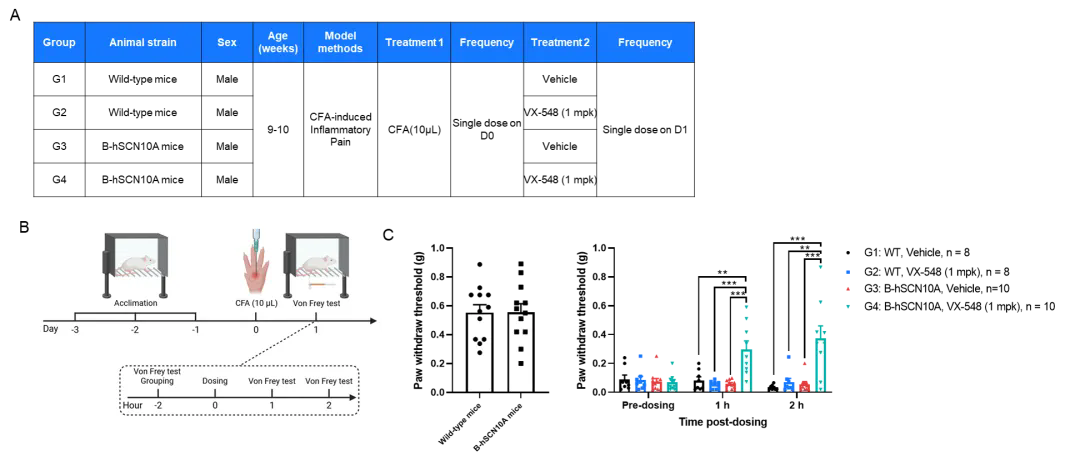
B-hSCN10A小鼠的机械痛阈值与野生型小鼠相似。在野生型小鼠和B-hSCN10A小鼠中,注射CFA(弗氏完全佐剂)均显著降低了机械痛阈值。在野生型小鼠中,1mpk(mg/kg)的VX-548未能缓解CFA诱导的炎症性疼痛。在B-hSCN10A小鼠中,1mpk的VX-548显著缓解了炎症性疼痛,且镇痛效果持续长达2小时。B-hSCN10A小鼠为靶向人SCN10A镇痛药物的体内药效评估提供了强大的临床前模型。(A) 分组与给药。(B) CFA诱导的炎症性疼痛造模示意图。(C) VX-548的镇痛效果。**P < 0.01, ***P < 0.001。
参考文献:
1.Ma RSY, Kayani K, Whyte-Oshodi D, Whyte-Oshodi A, Nachiappan N,Gnanarajah S,Mohammed R. Voltage gated sodium channels as therapeutic targets for chronicpain. J Pain Res. 2019 Sep 9;12:2709-2722. doi:10.2147/JPR.S207610. PMID:31564962; PMCID: PMC6743634.
2.Hameed S. Nav1.7 and Nav1.8: Role in the pathophysiology of pain. Mol Pain. 2019 Jan-Dec;15:1744806919858801. doi:10.1177/1744806919858801. PMID:31172839; PMCID: PMC6589956.