您可能也喜欢
高血压是最常见的心血管慢性疾病之一,其本质并非单一血压数值异常,而是由遗传易感性与环境因素共同作用下形成的复杂综合征,长期累及心、脑、肾及血管系统。由于疾病涉及多条调控通路,高血压研究和新药开发的关键,在于如何准确识别核心机制并验证靶点的真实作用。在这一背景下,研究思路正逐步从表型复制转向机制解析,动物模型的选择也随之发生变化。
从研究手段来看,高血压动物模型根据诱导方式主要可分为三大类:
遗传性高血压动物模型
手术诱导型高血压动物模型
药物诱导型高血压动物模型
其中,转基因高血压动物模型属于遗传性高血压模型的重要组成部分。该类模型通过将与高血压相关的外源基因整合至动物基因组,或对关键内源基因进行敲除或替换,从分子层面重构致病通路,为机制研究提供更高的通路特异性。
在众多血压调控通路中,肾素–血管紧张素–醛固酮系统(RAAS)及相关转运蛋白在血压稳态维持中发挥核心作用。该系统通过调节血管张力、钠水重吸收及体液容量维持血压稳态,其持续激活被认为是多种高血压类型的重要病理基础。
RAAS 的级联反应起始于两个关键分子——血管紧张素原(AGT)和肾素(REN)。在经典级联中,REN 由肾脏球旁细胞分泌,切割肝脏合成的 AGT 生成血管紧张素 I(Ang I),随后经血管紧张素转换酶(ACE)转化为血管紧张素 II(Ang II)。Ang II 作为主要效应分子,可促进血管收缩和醛固酮释放,从而引起血压升高。RAAS 不仅在生理性血压调节中发挥作用,其失衡也被确认参与高血压病理状态,并与多器官病变相关联[1]。
AGT 是该级联反应的底物来源,其表达水平升高为 Ang II 的生成提供基础条件,从而增强 RAAS 功能并推动血压升高。REN 则是级联反应的“启动开关”,其释放受肾灌注压、交感神经兴奋及钠负荷等多因素调控。当 REN 活性增加时,RAAS 整体被放大,导致 Ang II 和醛固酮水平升高,进一步引发外周血管阻力增加和体液容量扩增,显著提高血压水平。大量研究表明,AGT、REN 及其下游效应分子在高血压发生和进展中具有重要作用,这也是 ACE 抑制剂、AT1 受体拮抗剂等靶向药物临床应用的机制基础[2]。
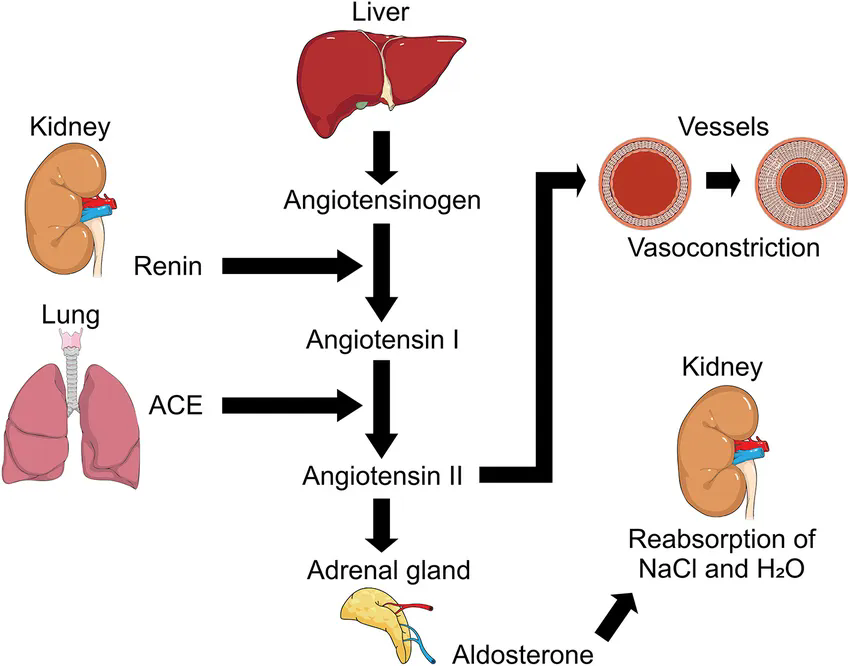
图1: RAAS 通过血管紧张素 II 介导的血管收缩调节动脉血压[3]
正因 RAAS 通路在高血压中的核心地位,围绕 AGT、REN 等关键节点构建的人源化小鼠和大鼠模型,逐渐成为机制研究的重要工具。与传统通过手术或药物诱导升压的模型相比,该类模型可在明确遗传背景下稳定调控单一通路,使血压变化与特定分子机制之间的因果关系更加清晰,在靶点验证、机制解析和新药研发中具有更高的转化潜力。
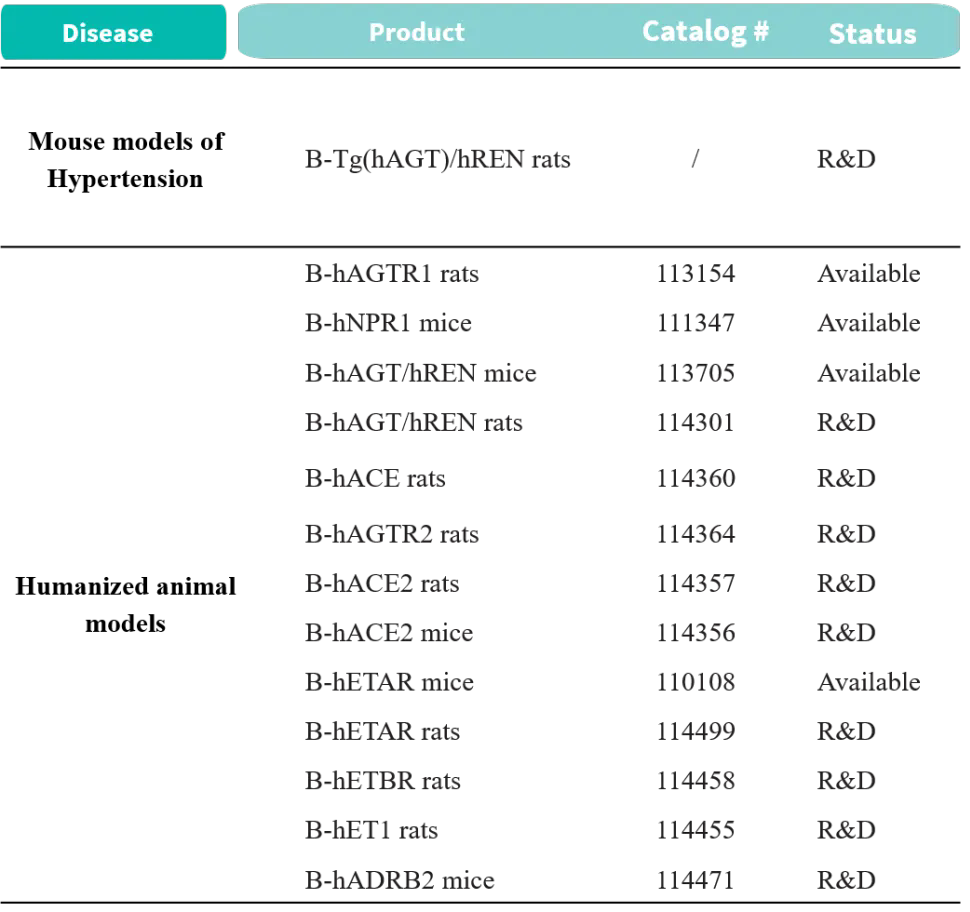
围绕 RAAS 相关核心通路,百奥赛图 构建了覆盖 AGT、REN、AGTR1、NPR1 等关键节点的转基因与人源化小鼠和大鼠模型体系,可支持从机制解析到药效评价的不同研究阶段。
mRNA 水平检测
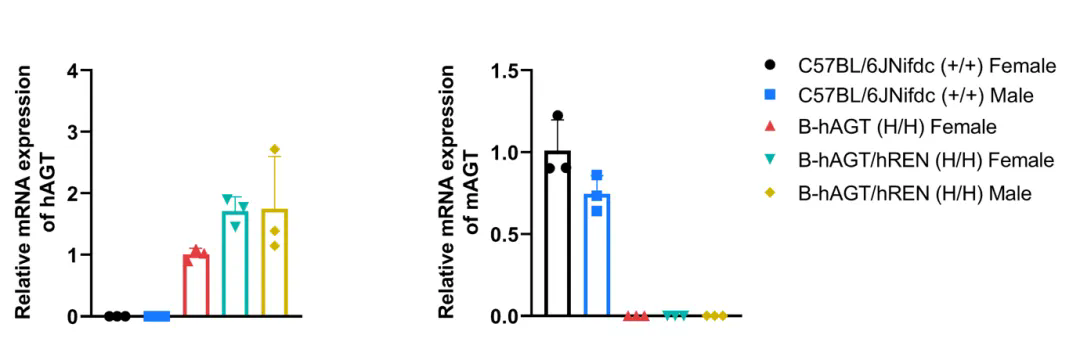
通过RT-qPCR分析野生型C57BL/6小鼠和B-hAGT/hREN小鼠中AGT基因表达。从野生型C57BL/6小鼠(雄性和雌性,N= 3,7周龄)和纯合B-hAGT/hREN小鼠(H/H; H/H)(雄性和雌性,N= 3,7周龄)的肝脏中提取RNA。qPCR分析鼠源和人源AGT的表达水平。鼠源Agt仅在野生型C57BL/6中检测到。人源AGT仅在纯合B-hAGT/hREN小鼠中检测到。数值以平均值±SEM表示。
蛋白表达检测
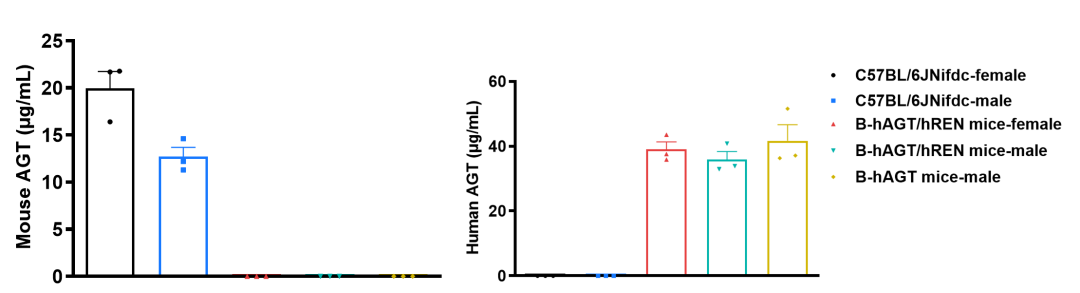
通过ELISA分析野生型C57BL/6、人源化B-hAGT纯合小鼠和人源化B-hAGT/hREN纯合小鼠AGT的表达。采集C57BL/6(雄性和雌性,n= 3,7周龄)、纯合B-hAGT小鼠(雄性,n= 3,7周龄)和纯合子B-hAGT/hREN小鼠(雄性和雌性,n= 3,7周龄)的血清。采用ELISA方法分析,鼠源AGT仅在野生型C57BL/6中表达。人源AGT仅在纯合B-hAGT小鼠和纯合B-hAGT/hREN小鼠中表达。数值以平均值±SEM表示。
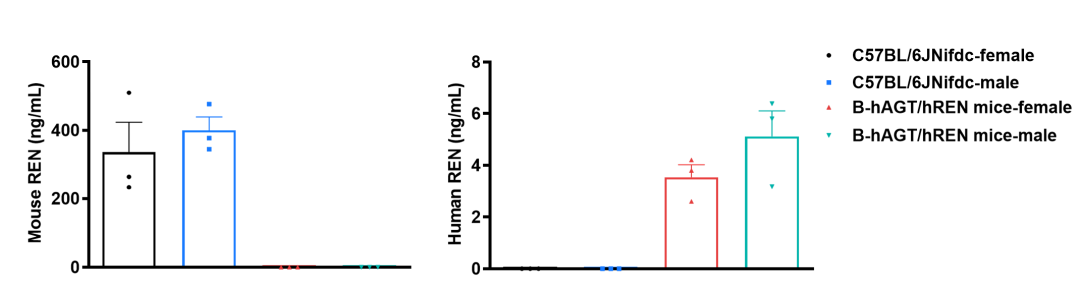
通过ELISA分析野生型C57BL/6、人源化B-hAGT纯合小鼠和人源化B-hAGT/hREN纯合小鼠REN的表达。采集C57BL/6(雄性和雌性,n= 3,7周龄)和纯合子B-hAGT/hREN小鼠(雄性和雌性,n= 3,7周龄)的血清。采用ELISA法分析,鼠源REN仅在野生型C57BL/6中表达。人源REN仅在纯合B-hAGT/hREN小鼠中表达。数值以平均值±SEM表示。
AGT 靶向核酸药物的抑制效率评估
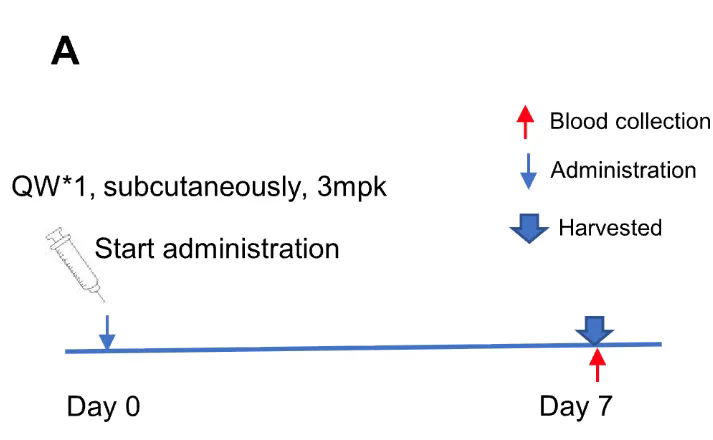
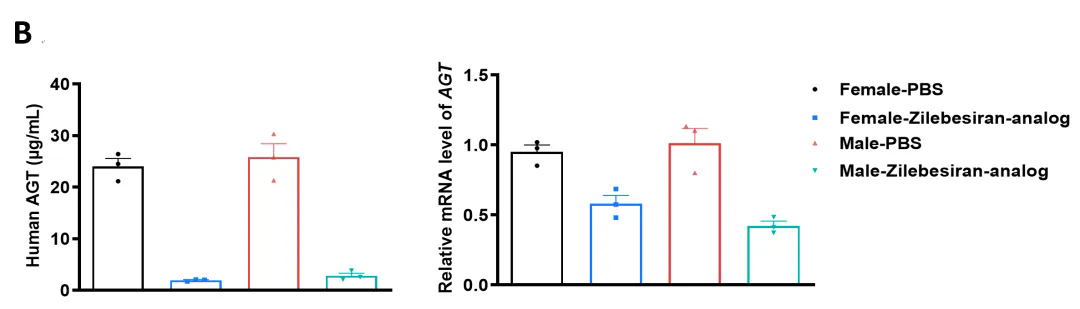
AGT靶向核酸药物对纯合子B-hAGT/hREN小鼠的抑制效果。B-hAGT/hREN小鼠随机分为4组(6-8周龄,雌性和雄性)。小鼠分别给予人AGT靶向核酸药物(Zilebesiran类似物)和PBS。第7天处死小鼠,取肝组织,ELISA检测人AGT蛋白表达水平,qPCR检测人AGT mRNA表达水平。A. 实验流程示意图。B. 治疗后肝脏中人AGT蛋白和人AGT mRNA的表达。与对照组相比,治疗组人AGT均明显降低,数值以平均值±SEM表示。
mRNA水平检测
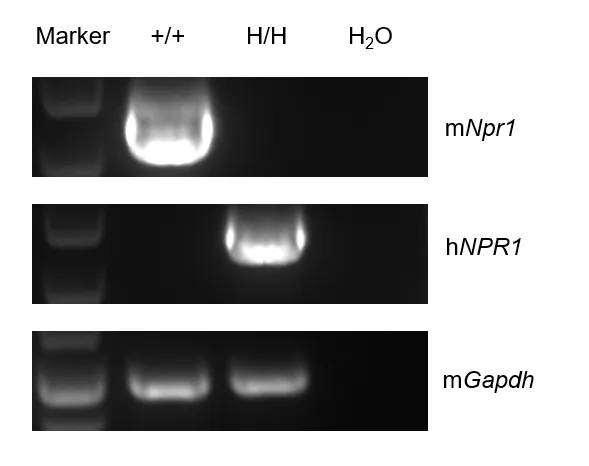
RT-PCR分析C57BL/6小鼠和B-hNPR1小鼠中npr1基因的表达。鼠源npr1 mRNA仅在野生型C57BL/6小鼠卵巢中表达。人源npr1 mRNA仅B-hNPR1小鼠(H/H)中表达。
蛋白表达检测
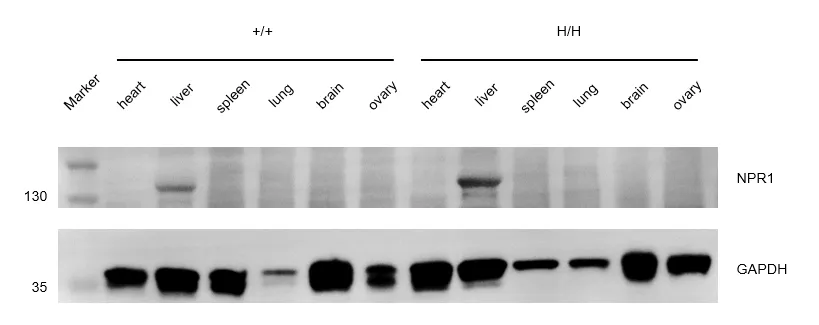
Western blot分析NPR1的表达。取野生C57BL/6小鼠(+/+)和纯合B-hNPR1小鼠(H/H)的心、肝、脾、肺、脑和卵巢,用已知的交叉反应性anti-NPR1抗体进行western blot分析。在野生C57BL/6小鼠和纯合B-hNPR1小鼠中均可检测到NPR1蛋白。
mRNA水平检测
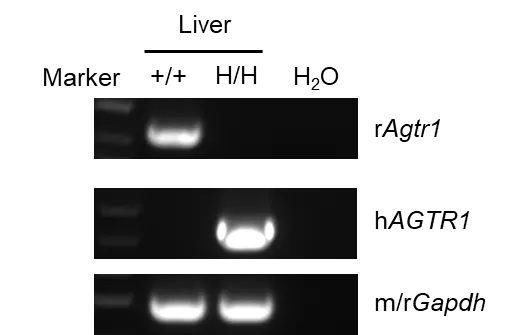
RT-PCR分析野生SD大鼠和B-hAGTR1大鼠中agtr1 mRNA的表达。从野生SD大鼠(+/+)和纯合B-hAGTR1大鼠(H/H)中分离肝脏RNA,反转录合成cDNA文库。鼠源agtr1 mRNA仅在野生型大鼠中表达。人源agtr1 mRNA仅在纯合B-hAGTR1大鼠表达。
蛋白表达检测
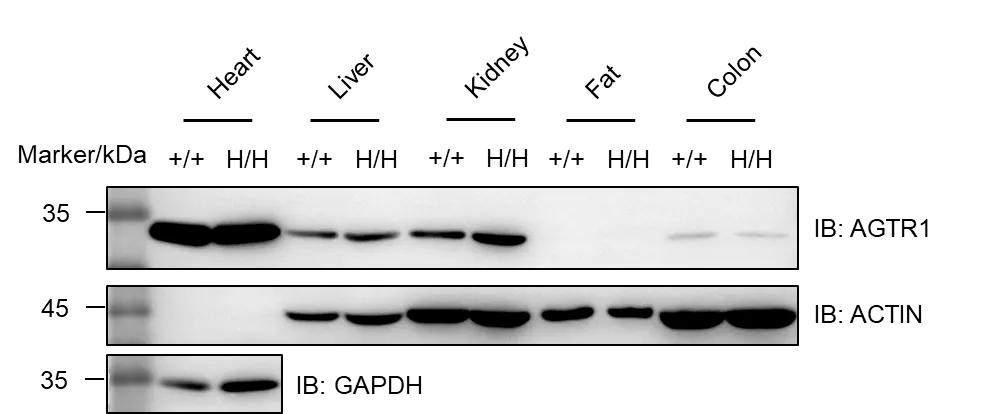
收集野生型SD大鼠(+/+)和纯合B-hAGTR1大鼠(H/H)的各组织器官的匀浆上清,用交叉反应anti-agtr1抗体(Abcam, ab124734)western blot分析。野生型大鼠和纯合子B-hAGTR1大鼠的心脏、肝脏和肾脏均检测到AGTR1,在结肠中检测到较弱AGTR1表达。
mRNA水平检测
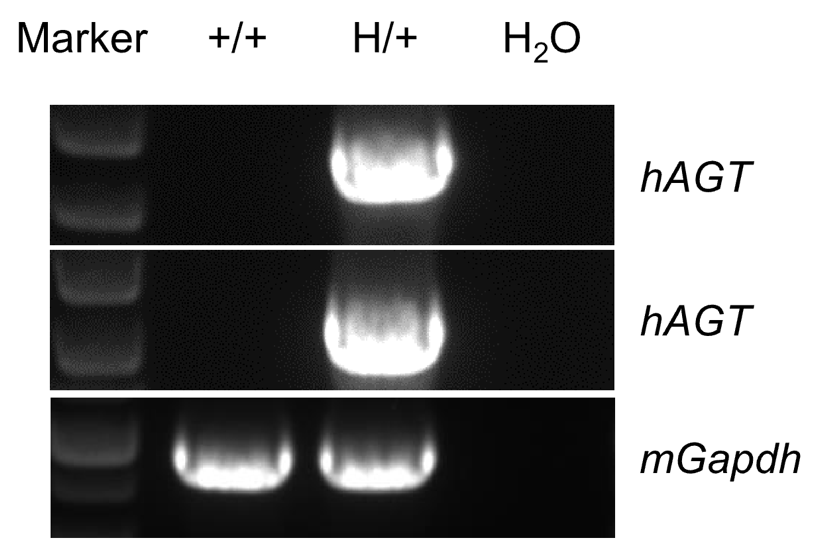
通过 RT-PCR 对野生型 C57BL/6小鼠与杂合B-hAGT 小鼠中AGT基因表达进行物种特异性分析。采集野生型 C57BL/6小鼠和杂合B-hAGT 小鼠的肝脏组织进行检测。结果显示,人源AGT mRNA 仅在杂合B-hAGT 小鼠中可检测到,而在野生型C57BL/6小鼠中未检测到。
蛋白表达检测
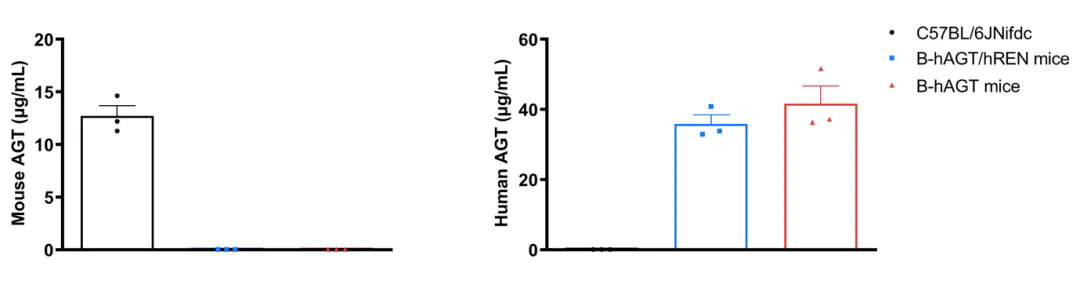
通过ELISA对野生型 C57BL/6小鼠、纯合人源化B-hAGT小鼠及纯合人源化B-hAGT/hREN小鼠中AGT表达进行品系特异性分析。采集野生型 C57BL/6小鼠(雄性,n = 3,7 周龄)、纯合B-hAGT 小鼠(H/H)(雄性,n = 3,7 周龄)以及纯合B-hAGT/hREN小鼠(雄性,n = 3,7 周龄)的血清样本。采用ELISA方法分别检测小鼠AGT和人源 AGT的表达水平。结果显示,小鼠AGT仅在野生型C57BL/6JNifdc小鼠中检测到;人源AGT仅在纯合B-hAGT小鼠和B-hAGT/hREN小鼠中检测到。数值以平均值±SEM表示。
AGT靶向核酸药物的抑制效率评估
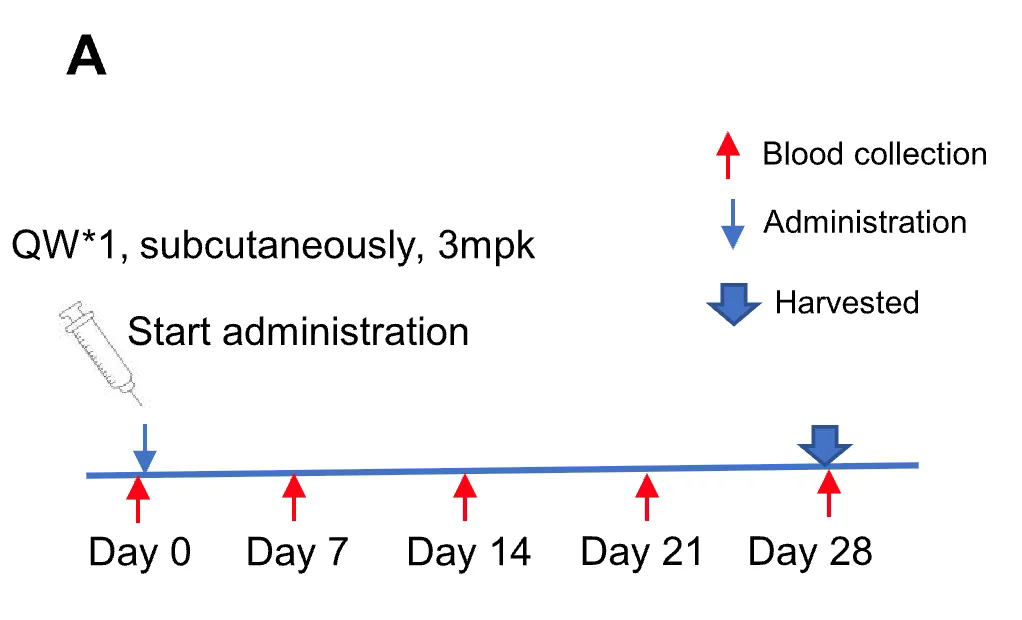
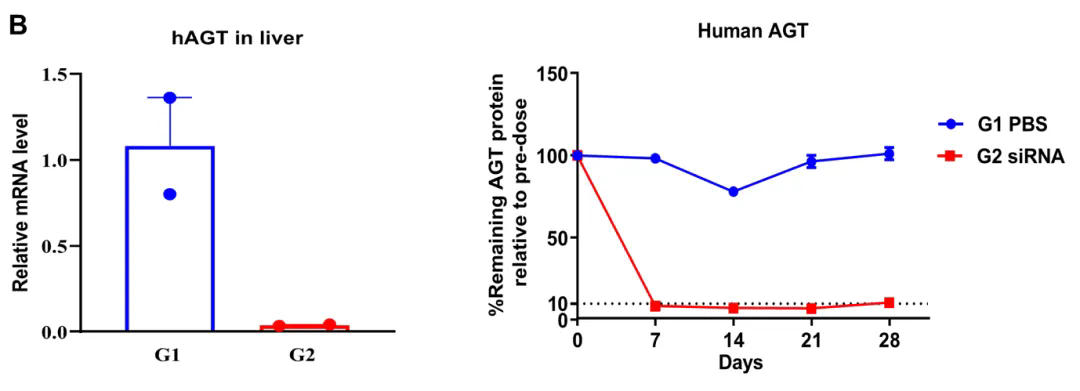
靶向AGT的核酸药物在纯合B-hAGT小鼠中的抑制效率评估。将纯合B-hAGT小鼠随机分为两组(6–8 周龄,雌性)。分别给予靶向人源AGT 的核酸药物(依据专利合成)或 PBS 对照处理。核酸药物以PBS水溶液形式给药。给药后第 28 天处死小鼠,采集肝脏组织,通过 qPCR 检测人源AGT mRNA的表达水平。(A)实验流程示意图。(B)给药后肝脏中人源AGT mRNA的表达水平,以及给药后第 7、14、21 和 28 天血浆中AGT蛋白表达水平相对于给药前的变化情况。结果显示,治疗组在人源AGT mRNA水平上的抑制率达到 96%。与对照组(G1)相比,治疗组(G2)中人源AGT表达显著降低,表明B-hAGT小鼠可作为评估靶向人源AGT核酸药物体内疗效的有力临床前模型。数值以平均值±SEM表示。
参考文献:
1.Pop D, Dǎdârlat-Pop A, Tomoaia R, Zdrenghea D, Caloian B, et al. Updates on the renin-angiotensin-aldosterone system and the cardiovascular continuum. Biomedicines 2024(12)7:1582.
2.Muñoz-Durango N, A Fuentes C, Castillo AE, González-Gómez LM, Vecchiola A, Fardella CE, Kalergis AM et al. Role of the renin-angiotensin-aldosterone system beyond blood pressure regulation: Molecular and cellular mechanisms involved in end-organ damage during arterial hypertension. International Journal of Molecular Sciences 2016;17(7):797.
3.Vargas-Rodriguez JR, Garza-Veloz I, Flores-Morales, V, Badilo-Almaraz JI, Rocha-Pizaña MR, Valdés-Aguayo JJ, Martinez-Fierro ML, et al. Hyperglycemia and angiotensin-converting enzyme 2 in pulmonary function in the context of SARS-CoV-2 infection. Frontiers in Medicine 2022;8:758414.