您可能也喜欢
过去十年,小核酸药物始终被视为潜力巨大的前沿技术,但其发展一度受限于递送效率、给药频率与规模化验证。近两年,随着小干扰 RNA(siRNA)和反义核苷酸(ASO)在心血管、代谢、肾病及中枢神经系统等领域持续交出具有确定性的临床数据,这一技术路径完成了从“机制可行”到“临床可行”,再到“商业可行”的关键跨越。
截至 2025 年,全球已获批小核酸药物共 23 款,其中 siRNA 7 款、ASO 14 款,覆盖 11 种罕见病,全年相关交易总额超过 270 亿美元。以 siRNA 领域的代表性企业为例,其核心产品在 2025 年上半年实现销售额 11.4 亿美元,同比增长 47%,显示小核酸药物的商业潜力正在快速释放。[4]
进入 2026 年,小核酸不再只是罕见病研发中的“技术验证工具”,而是开始系统性切入慢病与大人群适应症,包括心血管疾病、IgA 肾病、乙肝功能性治愈、减重代谢以及中枢神经系统疾病。资本活跃度与产业推进节奏的同步提升,标志着小核酸药物正进入以“平台化技术 + 多适应症并行”为特征的新阶段。
随着可选靶点数量不断增加,序列设计与化学修饰逐渐标准化,小核酸研发的竞争焦点正在发生变化。当前,真正决定项目质量与转化潜力的关键,不再只是是否实现基因沉默,而是能否在体内获得稳定、可重复、并与临床机制高度相关的药效数据。[4]
这意味着,小核酸药物评价标准已从“靶点敲降效率”,升级为“疾病表型是否得到实质改善”。在这一阶段,可靠的体内药效模型成为连接靶点机制与临床转化的核心基础设施。
小核酸药物的本质,是在蛋白翻译之前对 mRNA 进行精准调控。
siRNA 通过 RNA 诱导沉默复合体(RISC)介导的靶向切割,实现高效而特异的基因沉默;ASO 则可在转录后调控、剪接干预乃至翻译层面发挥作用。[1.2]
与小分子药物或抗体相比,小核酸的优势并不仅在于“可靶向传统难成药靶点”,更在于其作用路径更加直接——从基因层面影响蛋白表达,从源头干预疾病进程。随着递送体系与化学修饰技术不断成熟,siRNA 的作用时间显著延长,给药频率已从每日或每周,拓展至数月一次。这一变化,使小核酸药物在慢病领域首次具备结构性优势。
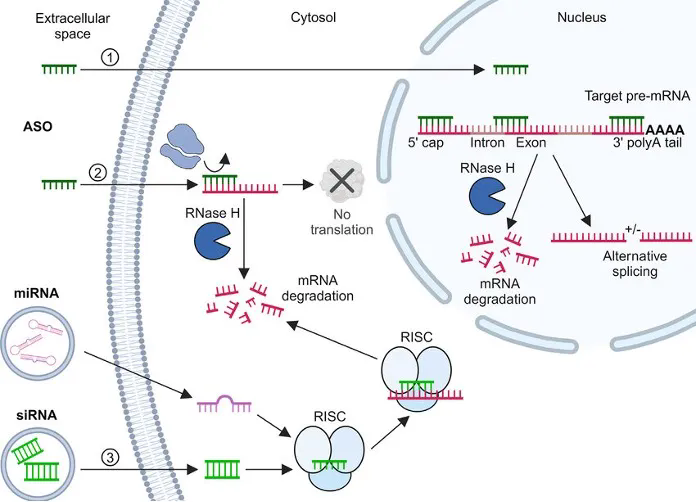
图1. ASO和siRNA的作用机制[3]
在已上市的小核酸药物中,PCSK9 与 APOC3 是最具代表性的成功靶点。
靶向 PCSK9 的 siRNA 药物在多项临床研究中实现了低密度脂蛋白胆固醇(LDL-C)的长期、稳定下降,并显著降低给药频率;而靶向 APOC3 的核酸药物,在高甘油三酯血症等适应症中持续改善血脂水平,验证了通过基因沉默调控脂代谢通路的临床可行性。[4]
这些成功案例同步抬高了研发门槛,也对前端药效评价提出了更高要求。
在减重与代谢领域,靶点往往同时影响能量代谢、脂肪分布及胰岛素敏感性,药效评估需超越单纯体重变化,更关注脂肪动员方式、代谢结构及长期可持续性。
在脂代谢领域,APOC3、PCSK9、LPA 等靶点的临床价值,取决于多通路联动下心血管风险的整体改善。其中 LPA 仅在人类和灵长类中表达,使人源化模型成为体内药效研究的必要前提[4]。
在中枢神经系统疾病领域,小核酸药物研发高度依赖对脑部递送效率、敲降深度、病理变化及行为学表型的系统性评估,而合适的体内模型是验证靶点干预与疾病改善因果关系的关键[3]。
围绕代谢、脂代谢及中枢神经系统等关键通路,百奥赛图构建了一系列针对核心靶点的小核酸药物药效评价人源化小鼠模型,可支持从靶点机制研究到体内药效验证的不同研发阶段。
这些模型为小核酸项目提供稳定、可重复的实验基础,同时可用于指导剂量选择和给药策略,从而降低临床转化风险。
核酸药物对人源INHBE的抑制效率

将B-hINHBE小鼠(雄性,7-8周龄)随机分为两组。分别给予靶向人源INHBE的核酸药物(根据专利合成)或PBS对照处理。给药后第14天处死小鼠,采集肝组织,采用qPCR检测人源INHBE mRNA的表达水平。(A) 实验流程示意图。(B) 通过qPCR检测人源INHBE mRNA的表达水平。与对照组相比,siRNA处理组中人源INHBE表达显著降低。
采用t检验进行统计学分析,*p < 0.05。数据以均值±SEM表示。
高脂饮食(HFD)诱导的B-hINHBE小鼠体内药效
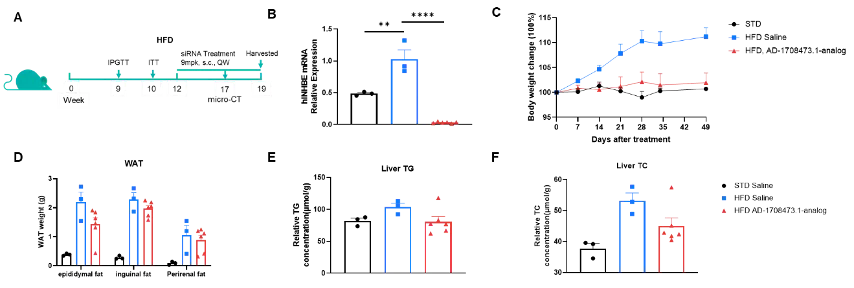
将B-hINHBE小鼠高脂饲养12周后根据体重分组,分别给予小鼠生理盐水和靶向人源INHBE的核酸药物(根据专利合成)。小鼠每周一次皮下给药,给药期间每周检测体重,。(A) 实验流程示意图。(B) 实验终点肝脏中INHBE的mRNA水平。(C) 治疗期间的体重变化。(D) 实验终点的白色脂肪质量变化。(E) 实验终点的肝脏甘油三酯变化。(F) 实验终点的肝脏总胆固醇变化。
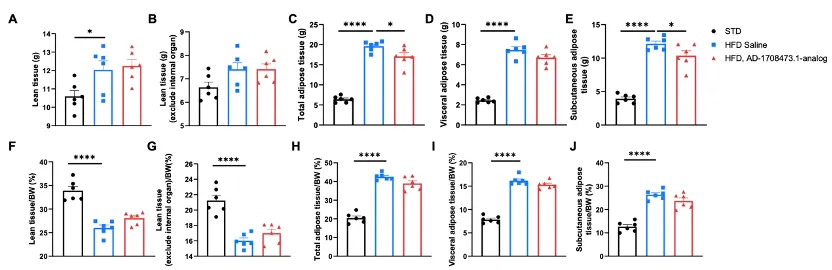
HFD诱导的B-hINHBE小鼠中INHBE-siRNA的药效研究。使用micro-CT 对小鼠进行3D重建分析在给药7次后对瘦体重和脂肪组织的变化。(A–E) 瘦组织重量、去除内脏后的瘦组织重量、总脂肪组织重量、内脏脂肪组织重量以及皮下脂肪组织重量。(F–J) 瘦组织占小鼠体重的百分比、去除内脏后的瘦组织占比、总脂肪组织占比、内脏脂肪组织占比以及皮下脂肪组织占比。
通过单因素方差分析(one-way ANOVA)进行统计,*P<0.05,**P<0.01,***P<0.001,****P<0.0001。
核酸药物对人源ALK7的抑制效率
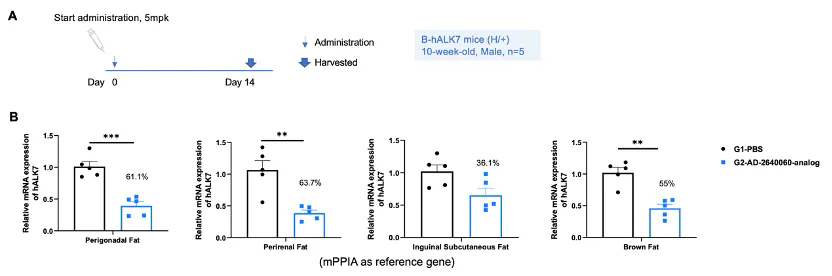
将B-hALK7小鼠(H/+,雄性,10周龄,n=5)随机分为两组。分别给予靶向人源ALK7的核酸药物(客户提供)或PBS对照处理。给药后第14天处死小鼠,收集脂肪组织,通过qPCR检测人源ALK7 mRNA的表达水平。(A) 实验处理示意图。(B) 脂肪组织中人源ALK7 mRNA的表达情况。
采用t检验进行统计学分析,*P<0.05,**P<0.01,***P<0.001。数据以均值±SEM表示。
核酸药物对人源LPA和PCSK9的抑制效率
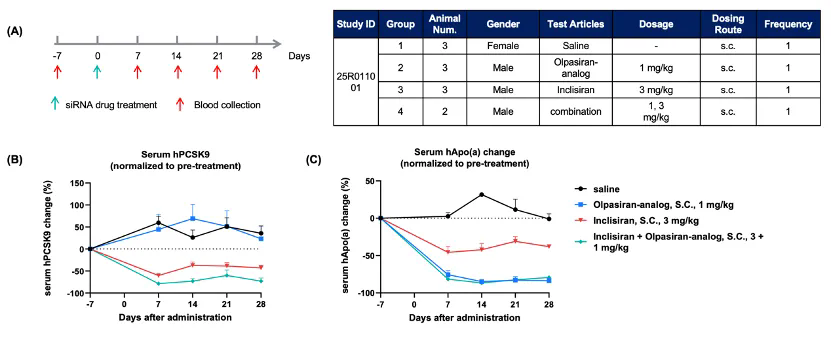
将 B-hLPA/hAPOB/hPCSK9 plus小鼠(6周龄)随机分为四组(每组n=2–3)。分别给予Olpasiran 类似物(由客户提供)、Inclisiran以及联合用药处理。给药后采集血清,检测Apo(a)和PCSK9的水平。(A) 实验流程示意图。(B)给药后人源PCSK9相对基线的平均变化百分比。(C) 给药后人源Apo(a)相对基线的平均变化百分比。数据以均值±SEM表示。
西方饮食(WD)诱导的B-hLPA/hAPOB/PCSK9 plus小鼠体内药效
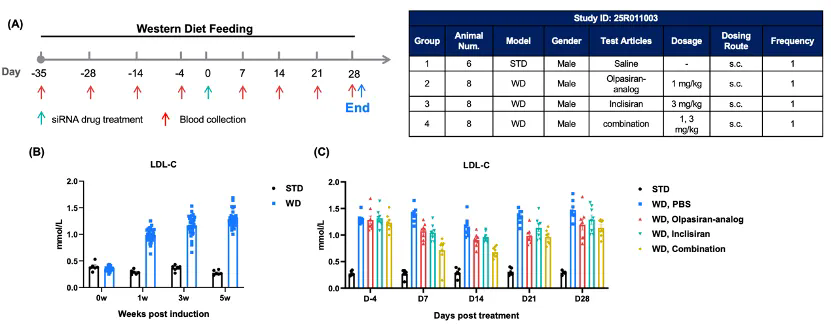
B-hLPA/hAPOB/hPCSK9 plus小鼠在实验开始时饲喂西方高脂饮食(Western Diet, XT079B,40%能量来自脂肪,胆固醇含量0.15%)5周,然后根据LDL-C水平将小鼠分为四组。分别给予Olpasiran类似物(根据专利合成),Inclisiran以及联合用药处理。(A) 实验流程示意图。(B) WD诱导后的LDL-C变化。(C) 给药后的LDL-C变化。数据以均值±SEM表示。
核酸药物对人源APP的抑制效率
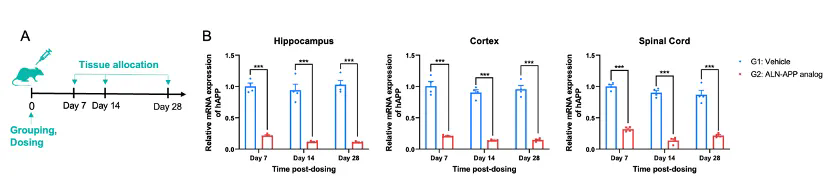
将B-hAPP*K670N*M671L*V717I小鼠(雄性,10周龄,n=4/组)随机分为两组。分别给予ALN-APP类似物(由客户提供)或人工脑脊液。小鼠在第7天、第14天和第28天被处死,收集海马体、皮层和脊髓组织,通过qRT-PCR检测人源APP mRNA的表达水平。(A) 实验流程示意图。(B) 海马体、皮层和脊髓中人源APP mRNA的表达情况。与对照组(G1)相比,处理组(G2)中人源APP mRNA显著降低,表明B-hAPP*K670N*M671L*V717I小鼠可作为评估人源APP靶向核酸药物体内药效的有效前临床模型。数据以均值±SEM表示。统计学分析采用非配对t检验,***P < 0.001。(本实验与客户合作)
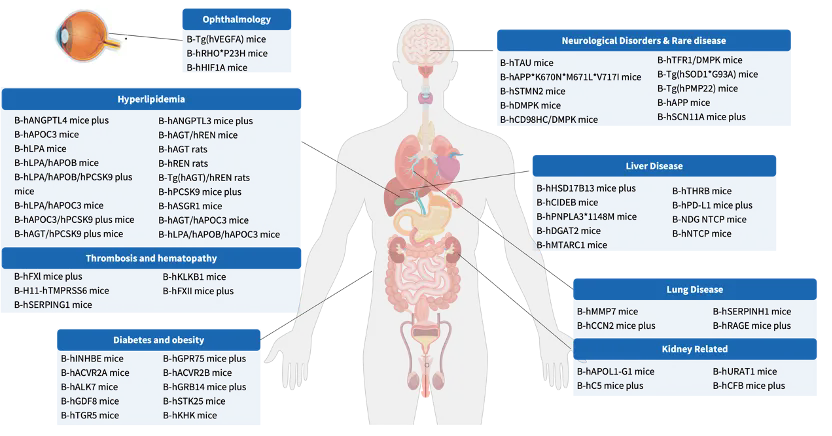
百奥赛图小核酸药物相关靶点人源化小鼠模型列表(部分展示)
参考资料
[1] Takakusa H, Iwazaki N, Nishikawa M, Yoshida T, Obika S, Inoue T. Drug Metabolism and Pharmacokinetics of Antisense Oligonucleotide Therapeutics: Typical Profiles, Evaluation Approaches, and Points to Consider Compared with Small Molecule Drugs. Nucleic Acid Ther. 2023;33(2):83-94. doi:10.1089/nat.2022.0054
[2] Hammond SM, Aartsma-Rus A, Alves S, et al. Delivery of oligonucleotide-based therapeutics: challenges and opportunities. EMBO Mol Med. 2021;13(4):e13243. doi:10.15252/emmm.202013243
[3] Chen KS, Koubek EJ, Sakowski SA, Feldman EL. Stem cell therapeutics and gene therapy for neurologic disorders. Neurotherapeutics. 2024;21(4):e00427. doi:10.1016/j.neurot.2024.e00427
[4] Liu M, Wang Y, Zhang Y, et al. Landscape of small nucleic acid therapeutics: moving from the bench to the clinic as next-generation medicines. Signal Transduct Target Ther. 2025;10(1):73. doi:10.1038/s41392-024-02112-8