您可能也喜欢
TCE(T-cell engager)正迎来快速发展阶段。随着三特异、多特异构型取得更多临床数据,TCE 已从血液瘤扩展至实体瘤和自身免疫疾病,呈现出多赛道共振的研发趋势。在这一过程中,能够真实反映人源化免疫反应的体内模型,成为推动创新加速转化的关键。
下文将从全球研发动态、TCE 结构逻辑、技术瓶颈,以及人源化模型在三特异 TCE 研发中的角色进行系统解析。
2025 年,TCE 在 ASCO、AACR 等国际会议上持续成为焦点,多家企业公布重要项目进展。
• AstraZeneca 展示 CD8 导向型三特异 TCE AZD5492,通过优先招募 CD8⁺ T 细胞,有望降低 CRS 风险[1]
• 泽璟制药三特异 TCE ZG006 在 SCLC Ⅱ期扩展研究中首次披露积极的临床信号[2]
• Boehringer Ingelheim 与 CDR Life 合作开发三特异抗体 CDR111,将 TCE 应用于自身免疫疾病[3]
TCE 正从单一适应症走向多领域的“多极扩展”。
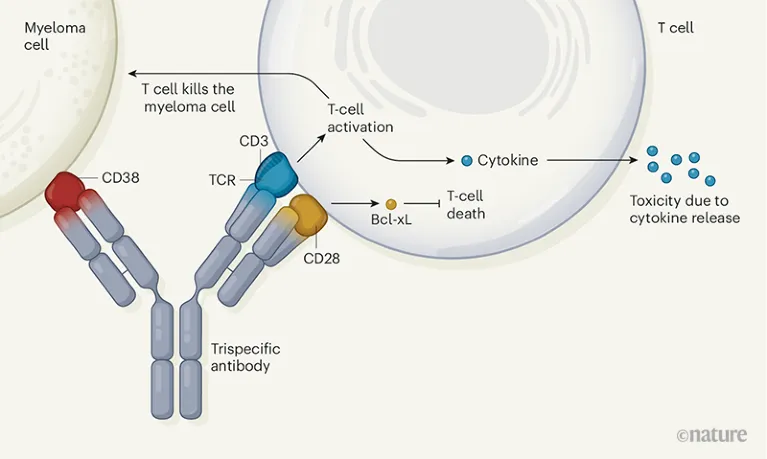
图1. 三特异性 TCE(CD3 × 肿瘤抗原 × 共刺激臂)结构示意[4]
• AbbVie 在 AACR 2025 披露 CD20×CD3×CD28 三特异 TCE 的临床前成果,展示共刺激信号的增强策略[5]
• Johnson & Johnson 强化 BCMA×CD3、CD38×CD3 双路径布局
• Regeneron 利用 Veloci-T 技术开发四特异 TCE,应对实体瘤抗原异质性[5]
• 齐鲁制药 QL615 成为国内首批进入临床的三特异 TCE[6]
• Enara Bio 推进靶向“暗抗原”的 ENA101 至 IND 阶段[7]
TCE 研发正从“双特异 × 血液瘤”向“多特异 × 实体瘤与免疫疾病”全面跨越。
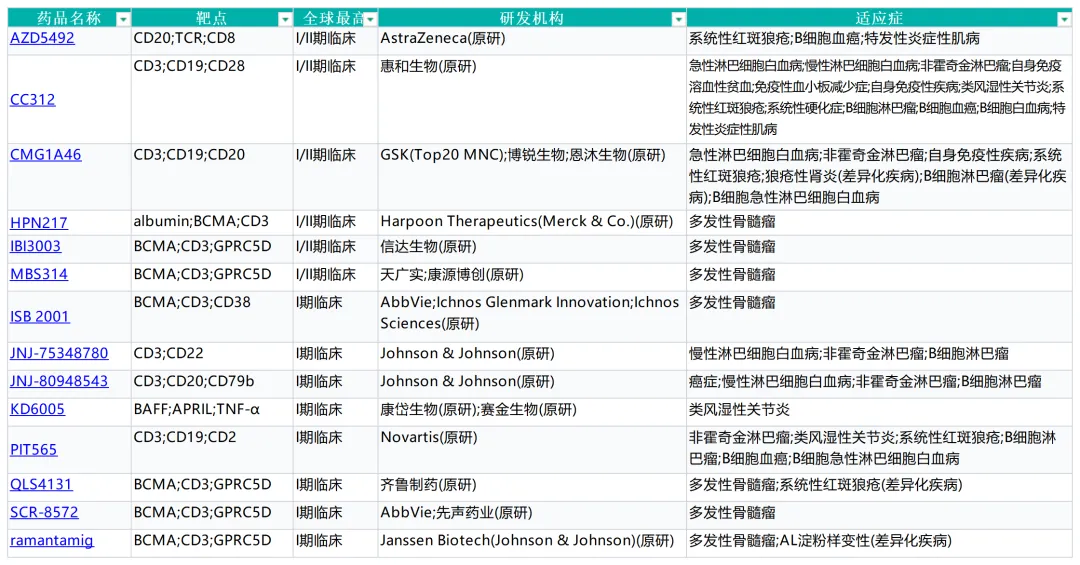
三特异 TCE 在传统“双抗”基础上加入第三功能臂,可为第二靶点或共刺激信号,实现更高控制力。
• “CD3 × 肿瘤抗原 × 共刺激信号(CD28/4-1BB)”
• “CD3 × 肿瘤抗原1 × 肿瘤抗原2(如 BCMA + CD38)”
其机制可推动 TCE 解决实体瘤常见挑战:
• 提升 T 细胞活化效率
• 延长 T 细胞持续杀伤
• 在异质性肿瘤中维持稳定免疫攻击
• 并在设计中努力降低 CRS 风险
临床证据方面,如 ISB 2001(BCMA × CD38 × CD3)在 RRMM 中取得 79% ORR[8]。
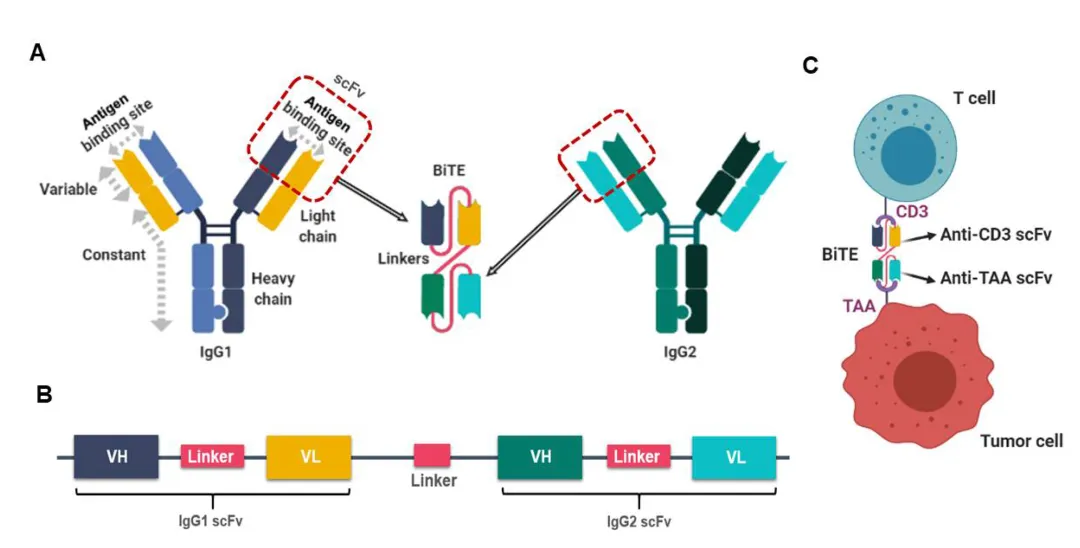
图2. 来自 Biochemistry K.H.U 的三特异抗体结构示意
三特异 TCE 的开发需要验证激活阈值、靶向性、CRS 风险、细胞毒性等核心参数。
能真实反映人源免疫反应的小鼠模型,因此成为“不可替代的验证基线”。
百奥赛图依托自主研发的人源化靶点小鼠,为多家全球药企的 TCE 项目提供支持,包括 CD3、EPCAM、CD20 等关键靶点。
以下展示部分模型及其应用数据。
Solitomab在B-hCD3EDG/hEPCAM小鼠体内的药效评价
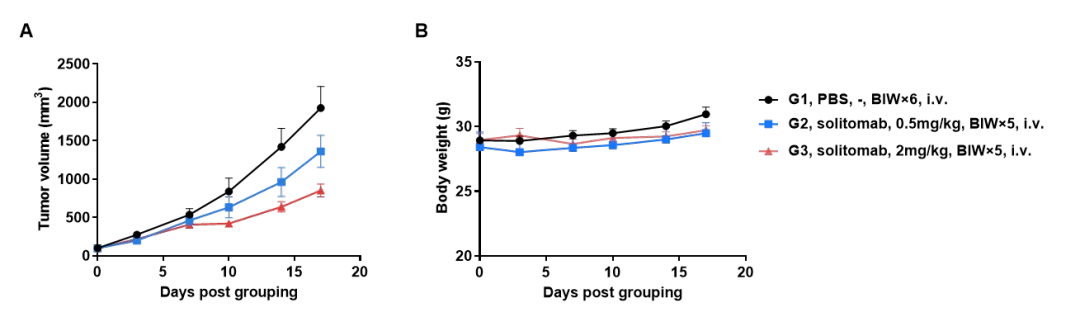
抗人CD3/EPCAM双特异性抗体(Solitomab类似物)在 B-hCD3EDG/hEPCAM 小鼠中的抗肿瘤活性。将B-hEPCAM MC38小鼠结肠癌细胞皮下接种于纯合B-hCD3EDG/hEPCAM小鼠(雄性,9 周龄,n = 6)。当肿瘤体积约达 100 mm³ 时,对小鼠进行分组,并静脉注射抗人CD3/EPCAM双特异性抗体(如图所示)。(A) 抗人CD3/EPCAM双特异性抗体可抑制 B-hEPCAM MC38 肿瘤在B-hCD3EDG/hEPCAM小鼠中的生长。(B) 治疗期间体重变化。数值以平均值 ± 标准误(SEM)表示。
Glofitamab在B-hCD3EDG/hCD20小鼠体内的药效评价
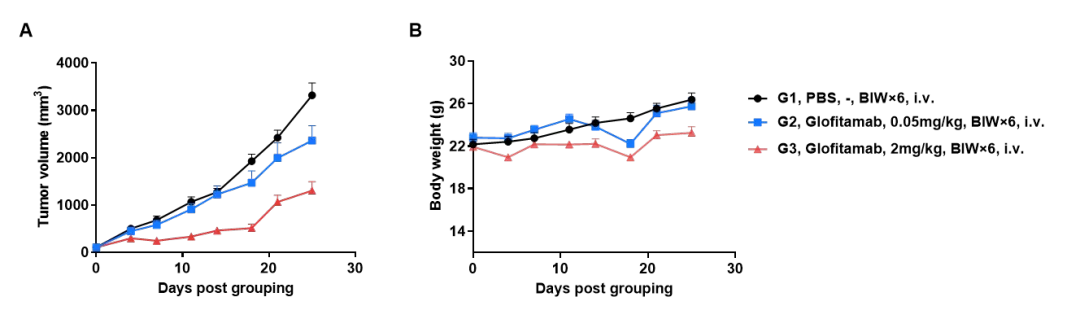
抗人CD3/CD20双特异性抗体(Glofitamab市售)在B-hCD3EDG/hCD20小鼠中的抗肿瘤活性。将B-hCD20 MC38小鼠结肠癌细胞皮下接种于纯合B-hCD3EDG/hCD20小鼠(雌性,9 周龄,n = 6)。当肿瘤体积约达 100 mm³ 时,对小鼠进行分组,并静脉注射抗人CD3/CD20双特异性抗体(如图所示)。(A) 抗人 CD3/CD20 双特异性抗体可抑制B-hCD20 MC38肿瘤在B-hCD3EDG/hCD20小鼠中的生长。(B) 治疗期间体重变化。数值以 平均值 ± 标准误 (SEM) 表示。
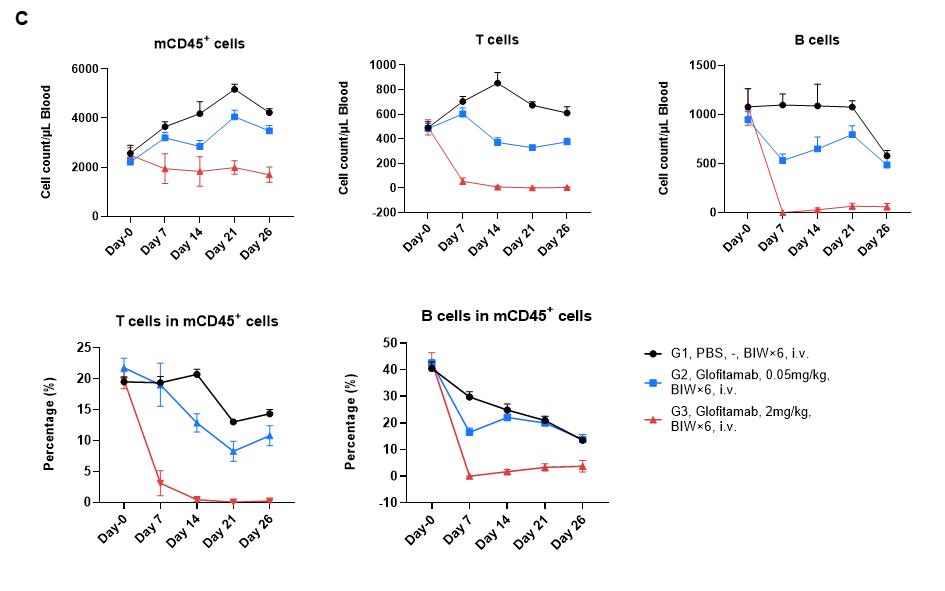
(C)抗CD3/CD20双特异性抗体 Glofitamab 可清除携带 B-hCD20 MC38 肿瘤的B-hCD3EDG/hCD20小鼠外周血中的 B 细胞。于分组后第 0、7、14、21 和 26 天采集血液样本。通过流式细胞术检测mCD45⁺细胞、B细胞(mCD19⁺)及T细胞(mTCRβ⁺)的数量和比例。结果显示,Glofitamab可有效清除B细胞,并诱导B-hCD3EDG/hCD20小鼠的T细胞死亡。数值以平均值±标准误(SEM)表示。
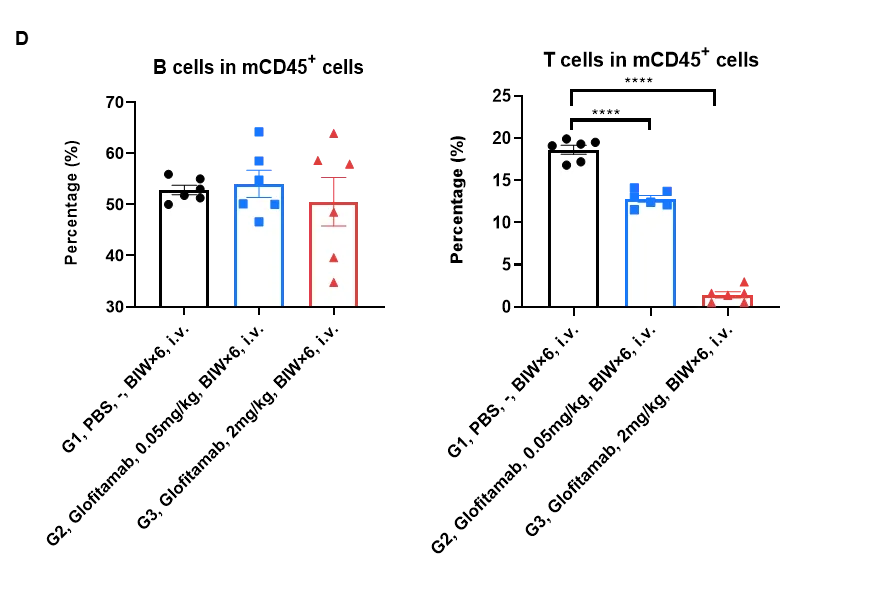
(D) 实验结束,收集脾脏细胞,并通过流式细胞术检测mCD45⁺细胞中B细胞(mCD19⁺)和T细胞(mTCRβ⁺)的比例。结果显示,Glofitamab可有效诱导T细胞死亡,但未能清除B-hCD3EDG/hCD20小鼠的B细胞。数值以平均值 ± 标准误(SEM)表示。显著性差异采用常规单因素方差分析(Ordinary one-way ANOVA)计算:*P < 0.05,**P < 0.01,***P < 0.001。
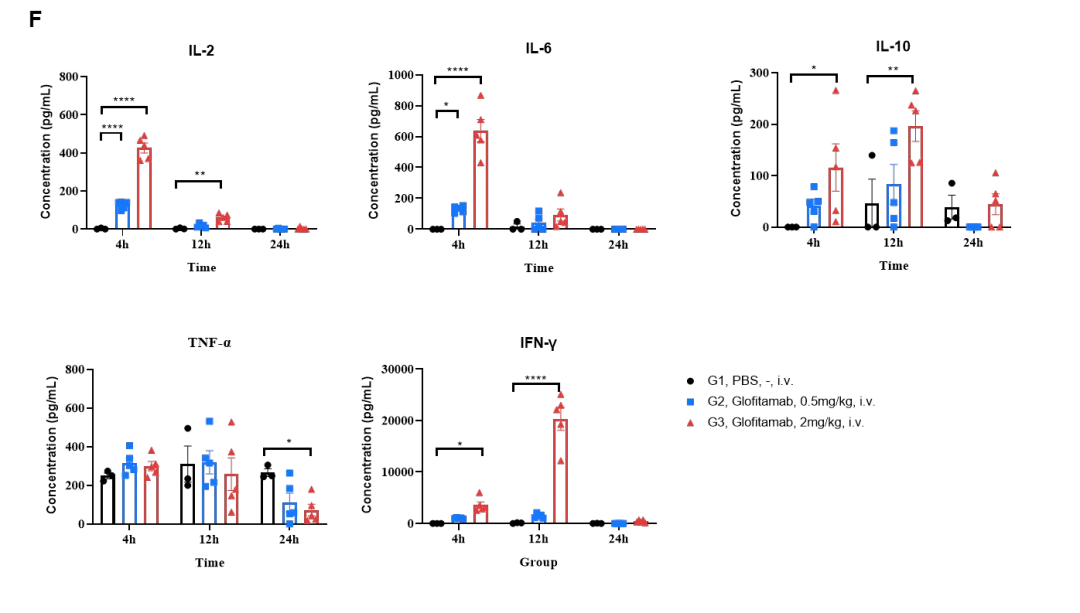
(F) 抗CD3/CD20双特异性抗体在携带B-hCD20 MC38肿瘤的B-hCD3EDG/hCD20小鼠中诱导细胞因子释放。于首次给药后4、12、24小时采集血液样本。数值以平均值±标准误(SEM)表示。显著性差异采用双因素方差分析(two-way ANOVA)检验:*P < 0.05,**P < 0.01,***P < 0.001。
该模型可用于探索:
• B 细胞清除能力
• T 细胞变化趋势
• CRS 风险评估
• 剂量反应关系
参考资料
[1]Hematology Advisor. Novel CD8-Directed Trispecific T-Cell Engager AZD5492 May Reduce Toxicity in Large B-Cell Lymphoma. Hematology Advisor. 2025. Available from:
https://www.hematologyadvisor.com/news/lymphoma-dlbcl-toxicity-novel-tri-specific-tcell-engager/
[2]American Society of Clinical Oncology (ASCO). ISB 2001 (BCMA × CD38 × CD3) in Relapsed/Refractory Multiple Myeloma (TRIgnite-1 Study). J Clin Oncol. 2025;43(Suppl 16). Available from: https://iginnovate.b-cdn.net/igi_pdfs/publications/ASCO%202025-%20Oral%20Presentation%20Final%202.pdf
[3]Business Wire. Boehringer Ingelheim and CDR Life Expand Collaboration Efforts with Global Licensing Agreement for CDR111, an Antibody-Based Trispecific Modulator for Autoimmune Diseases. Business Wire. November 4, 2025. Available from: https://www.businesswire.com/news/home/20251104115074/en/
[4]Callaway E. Antibody therapies go three-pronged to fight cancer.Nature. 2019;576(7785):S10–S11. doi:10.1038/d41586-019-03495-3
[5]BusinessWire. Boehringer Ingelheim and CDR Life Expand Collaboration Efforts with Global Licensing Agreement for CDR111, an Antibody-Based Trispecific Modulator for Autoimmune Diseases. BusinessWire News Release. November 4, 2025. Available from: https://www.businesswire.com/news/home/20251104115074/en/
[6]ASCO Abstract #8007. Phase II Expansion Study of ZG006 (DLL3 × CD3 Trispecific T-Cell Engager) in Extensive-Stage Small Cell Lung Cancer (ES-SCLC). J Clin Oncol. 2025;43(Suppl 16). Available from: https://ascopubs.org/doi/10.1200/JCO.2025.43.16_suppl.8007
[7]Qilu Pharmaceutical Co., Ltd. Announcement on Clinical Trial Approval of Trispecific T-Cell Engager QL615. National Medical Products Administration (NMPA), Center for Drug Evaluation (CDE) Bulletin. March 2025. Available from: https://www.qilu-pharma.com/news/2025QL615.html
[8]GlobeNewswire. Enara Bio’s DARKFOX Discovery Propels ENA101, the First-Ever Bispecific T-Cell Engager Targeting a Cancer-Specific Dark Antigen, into IND-Enabling Studies. GlobeNewswire Press Release. November 4, 2025. Available from: https://www.globenewswire.com/news-release/2025/11/04/3180455/0/en/