您可能也喜欢
在胰腺癌、胃癌等高风险肿瘤中,恶病质发生率可达60%–80%,显著降低患者生存质量并加速疾病进展。临床需求迫切,但目前仍缺乏真正针对病理机制的获批疗法,使癌症恶病质成为肿瘤支持治疗中尚未被充分满足的重要领域。可靠、可转化的动物模型,是将机制研究与药效验证连接到临床的关键一步。本文聚焦化学诱导、同源肿瘤、CDX三大经典恶病质模型,结合建模数据与药效案例,给出从模型构建到疗效验证的发布级参考。
癌症恶病质(Cancer Cachexia)是一种多因素代谢综合征,主要表现为进行性体重下降,尤其是骨骼肌与脂肪组织丢失,且常规营养支持难以逆转[1]。该综合征在晚期癌症患者中常见,部分实体瘤发生率可达80%,并与约20%癌症患者直接死亡相关[2]。
恶病质会显著影响生活质量,降低放化疗耐受性,增加治疗相关并发症与感染风险,最终导致多器官功能障碍甚至死亡[3]。尽管相关临床试验众多,目前除日本批准Anamorelin用于特定癌症恶病质治疗外,全球范围内仍缺乏FDA批准的上市药物[4]。临床前到临床转化的高失败率,进一步提示动物模型必须更贴近人类疾病状态与可测终点[5]。
恶病质是多系统失衡的结果,可归纳为五个相互耦合的机制模块(见图1):
系统性炎症反应:肿瘤微环境与免疫细胞释放促炎因子,如IL-6、TNF-α等
免疫失衡:肿瘤相关免疫调节导致慢性炎症持续
代谢紊乱:能量消耗增加,蛋白质降解与脂解增强
神经内分泌失调:下丘脑-垂体轴异常,影响食欲与代谢
能量负平衡:摄入减少与消耗增加共同驱动体重下降
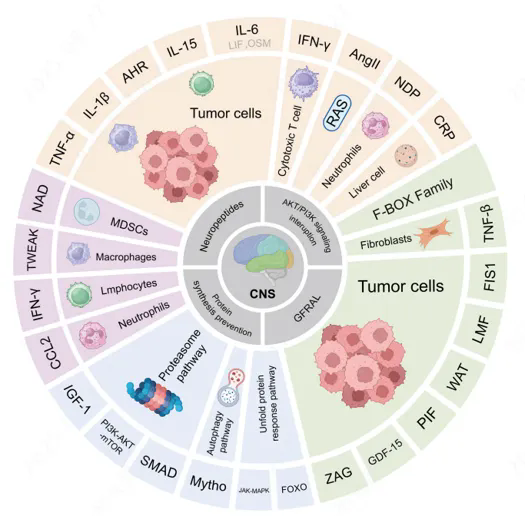
图1. 癌症恶病质多机制相互作用示意图[6]
近年研究显示,生长分化因子15(GDF15)在多种癌症中高表达,并与恶病质严重程度相关。与非恶病质患者相比,恶病质患者血浆GDF15水平可显著升高,且高GDF15水平与生存期缩短相关[7]。肿瘤细胞中MAP3K11/MLK3通路激活,可上调GDF15表达与分泌。循环GDF15可通过中枢受体GFRAL抑制食欲,并促进肌肉蛋白降解与脂肪分解,从而推动全身消耗(图2)[8]。
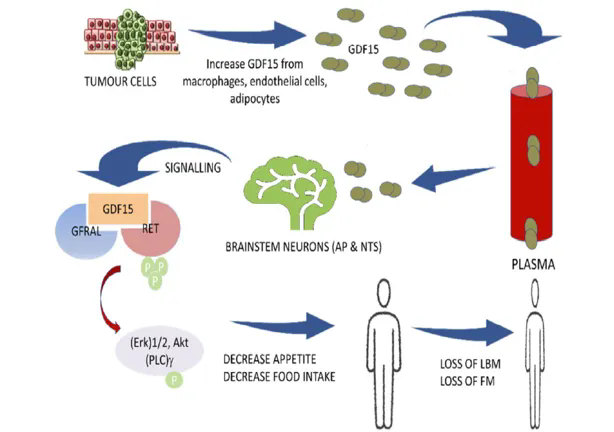
图2. GDF15在驱动癌症恶病质中的作用[8]
临床前研究表明,中和GDF15可在多种恶病质模型中改善体重下降、肌肉萎缩与脂肪丢失,并提升生存表现[9]。因此,围绕GDF15的可转化药效体系,成为恶病质药物研发的重要路径之一。
临床前恶病质模型常见五类体系(图3):
移植模型:同种移植(如C26、LLC)与异种移植(CDX如HT-1080等;PDX为患者来源)
转基因/自发模型:如ApcMin/+、KPC等
化学诱导模型:化疗药物诱导消耗表型(如顺铂等)
其他动物模型:斑马鱼、果蝇等
细胞模型:条件培养基或特定因子诱导萎缩
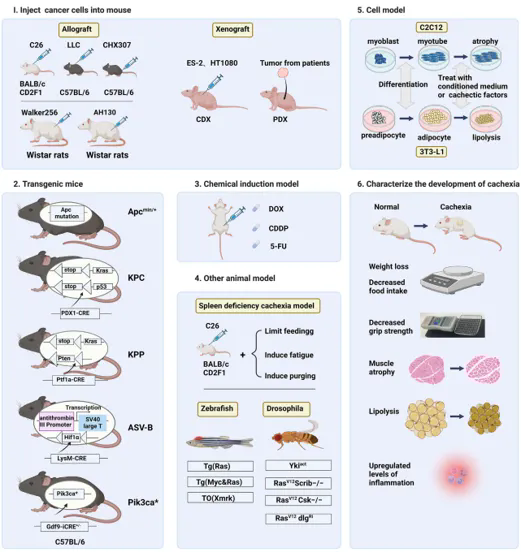
图3. 癌症恶病质主要临床前研究模型分类[1]
不同模型的共同表型建议采用“可转化终点”组合评估:
体重:总重与去瘤体重(肿瘤模型必选)
摄食量:用于区分厌食主导与代谢消耗主导
体成分:Lean mass与Fat mass(建议纵向追踪)
组织终点:腓肠肌、股四头肌等肌肉重量;白脂组织重量
形态学:肌纤维横截面积(H&E)
机制标志物:炎症因子、GDF15等循环指标
百奥赛图可提供多类型癌症恶病质动物模型与配套表型检测,覆盖模型构建、表型评估与药效验证的全流程临床前研究服务。
选择模型时,建议先回答三件事:
1)药物机制更接近“化疗相关消耗”还是“肿瘤驱动消耗”?
2)是否需要完整免疫系统参与(免疫调节、炎症网络、联合免疫治疗)?
3)药物靶点是否人源特异(需要人源GDF15/人源抗体等交叉反应)?
对应关系可概括为:
化学诱导模型:适合快速验证“系统性消耗”与对症改善能力
同源肿瘤模型:适合评估肿瘤-免疫-代谢联动与免疫相关机制
CDX模型:适合验证人源靶点通路与人源生物标志物可追踪性
化学诱导恶病质模型通过注射化疗药物(如顺铂)诱导体重下降与组织消耗,优势在于周期短、变异小、便于快速筛选。该模型特别适合:
化疗相关消耗或食欲抑制机制研究
以体重与体成分改善为主要终点的候选药物筛选
生物标志物(如GDF15)与表型联动验证
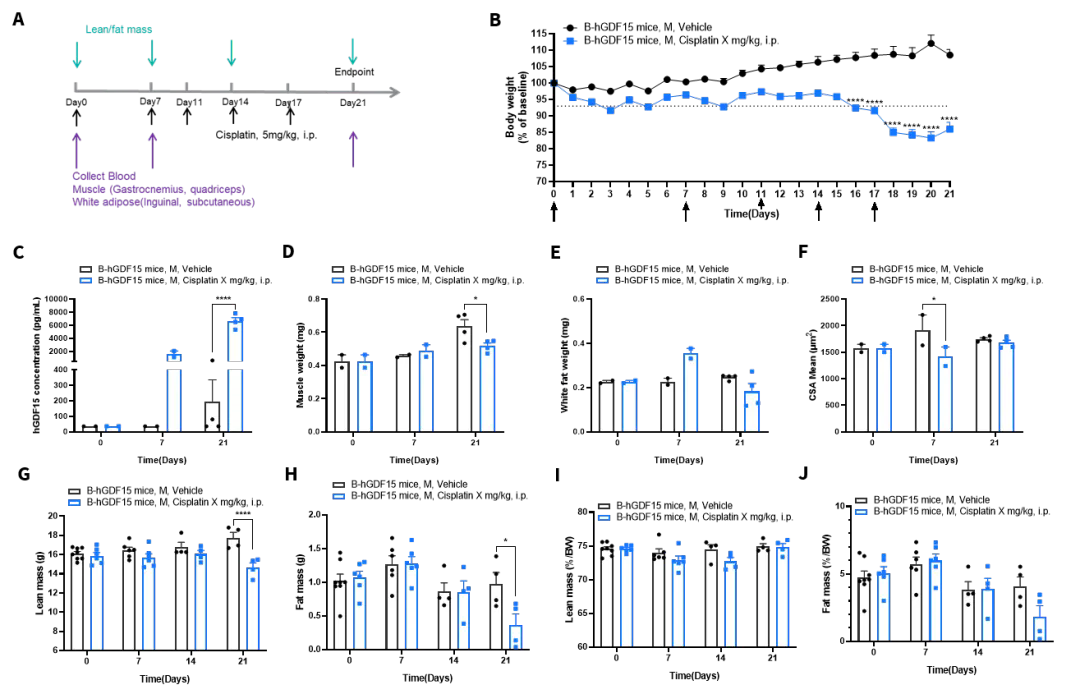
图4. 化学诱导恶病质模型造模数据
如图4所示,百奥赛图利用B-hGDF15转基因小鼠构建了Cisplatin诱导的恶病质模型。在提高给药频率(三针强化方案)后,小鼠体重显著下降至初始体重的93%(图4B,虚线示意),表明系统性消耗状态已成功诱导。造模第21天实验结束时,从小鼠身上采集了多项生理与组织样本以全面评估恶病质表型。
通过体脂仪检测Lean mass与Fat mass,两项结果均显著降低,显示小鼠肌肉与脂肪同步丢失。小鼠安乐死前进行采血,经ELISA检测证实小鼠循环中hGDF15浓度显著上升(图4 C),提示GDF15在化学诱导恶病质中可能起关键调控作用。小鼠的骨骼肌(腓肠肌、股四头肌)重量显著降低;白色脂肪组织(腹股沟、皮下脂肪)重量也呈下降趋势(图4 D、E)。小鼠骨骼肌进行 H&E 染色,显示肌纤维横截面积明显减少(图4F),从形态学层面证实肌肉萎缩的发生。
综上,本研究通过 Cisplatin 高频给药在B-hGDF15小鼠中成功构建了伴有GDF15升高的恶病质模型,系统验证了其在体重、体成分、血液标志物、组织重量及病理形态等方面的典型消耗表型,为后续机制研究与药物评价提供了可靠的工具。
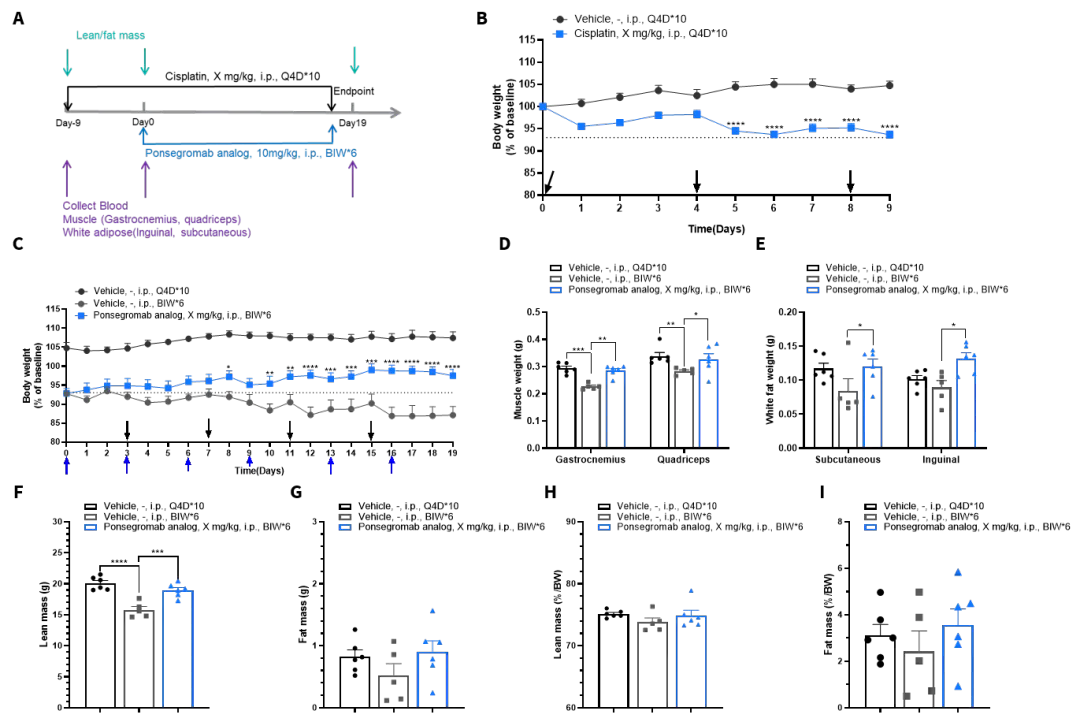
图5. 化学诱导恶病质模型药效数据
在成功建立Cisplatin诱导的恶病质模型后,我们进一步开展了药效研究(图5)。小鼠在体重显著下降后(图5B,造模至分组前数据),被随机分为治疗组与对照组,并接受为期三周的干预。
治疗组小鼠给予 Ponsegromab(腹腔注射,每周两次,共计6次),而对照组给予相应溶剂。干预期间持续监测体重变化,结果如图5C 所示,治疗组小鼠体重下降趋势得到明显缓解,表明Ponsegromab具有改善恶病质相关体重丢失的潜力。
实验终点时,治疗组小鼠的Lean mass与Fat mass较对照组均有所回升,骨骼肌(腓肠肌、股四头肌)重量也增加,白色脂肪组织(腹股沟、皮下脂肪)重量也呈现恢复趋势,提示Ponsegromab在该Cisplatin诱导的恶病质模型中表现出改善体重丢失、维持体成分的药效潜力,为后续针对GDF15相关靶点的抗恶病质药物开发提供了临床前依据。
主要终点:体重变化(相对基线)、Lean mass变化
关键支持:摄食量、Fat mass、循环GDF15(或相关标志物)
组织终点:骨骼肌重量与肌纤维横截面积
质量控制:给药频率、脱水/肾毒性等非特异性因素排除
同源肿瘤恶病质模型将小鼠源肿瘤细胞接种至同品系免疫健全小鼠,能保留肿瘤-免疫互作与炎症网络,更适合:
免疫相关机制(炎症、细胞因子网络)验证
抗恶病质药物与抗肿瘤/免疫治疗联合评估
区分“抑制肿瘤生长”与“改善消耗表型”的独立贡献
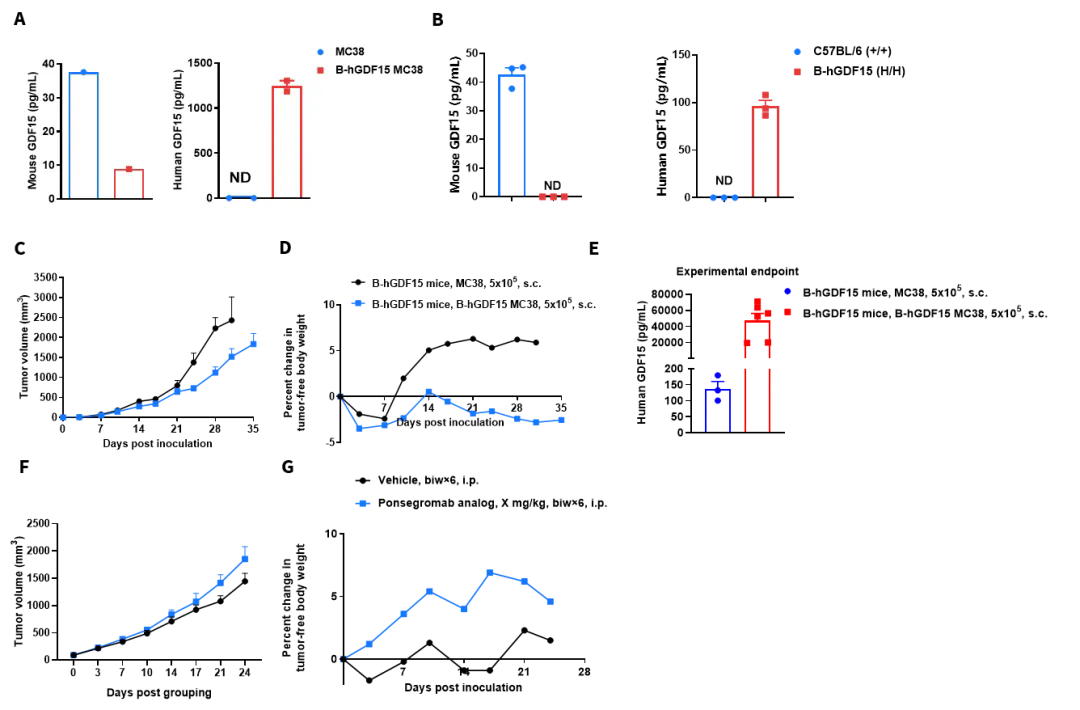
图6. 靶点人源化细胞和小鼠造模及药效数据
为了加速靶向GDF15的癌症恶病质药物研发,百奥赛图成功构建了关键的研究工具:靶点人源化的B-hGDF15 MC38细胞株与B-hGDF15小鼠。如图6A所示,改造后的B-hGDF15 MC38细胞株,其培养上清中能检测到高表达的hGDF15。同时,B-hGDF15小鼠的基础血清中也可检测到hGDF15(图6B)。
我们尝试模拟了GDF15驱动的恶病质进程:将B-hGDF15 MC38细胞接种于B-hGDF15小鼠后,肿瘤稳定生长(图6C),去瘤体重与对照组(野生MC38)相比显著下降(图6D,尽管未能检测到与自身初始体重比显著下降的体重(丢7%初始体重)),同时血清中hGDF15水平急剧升高(图6E)。治疗性干预结果显示,hGDF15靶向治疗并不会抑制肿瘤生长(图6F),但能显著逆转体重下降趋势(图6G),证明了该模型在药效评估中的实用价值。
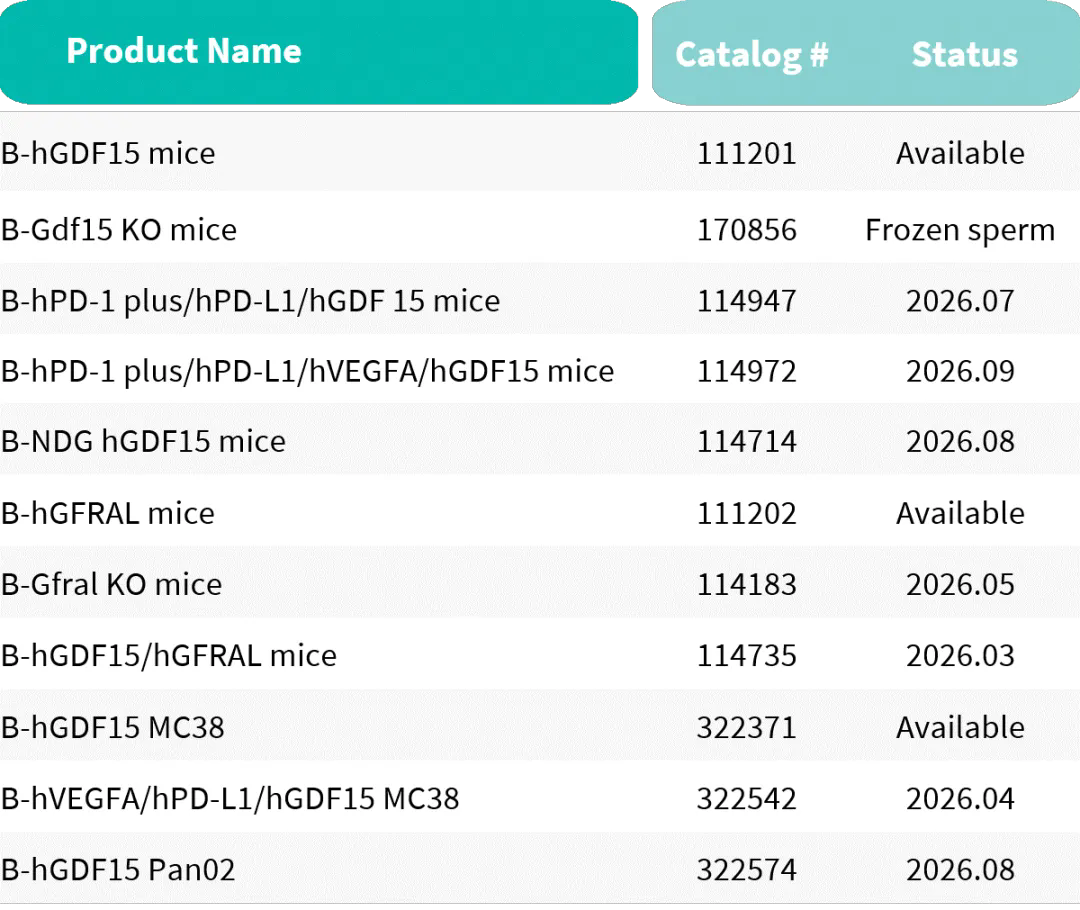
到目前为止,围绕hGDF15靶点的完整临床前研究产品体系(图6H)已成功建立,涵盖从基因人源化细胞、人源化动物模型到相应的表型检测,旨在为学术界与工业界提供一站式的解决方案,共同推进恶病质新药的开发。
必选:去瘤体重、肿瘤生长曲线
建议:摄食量与炎症因子谱,辅助解释机制
终点:肌肉/脂肪组织重量、H&E横截面积
结论表达:明确“对肿瘤生长影响”与“对消耗表型改善”两条证据链分离呈现
CDX恶病质模型将人源肿瘤细胞移植至免疫缺陷小鼠,适合研究人源特异性靶点与人源分泌因子驱动的消耗表型。对于GDF15驱动型恶病质,CDX模型的转化优势在于:
血浆可直接检测人源GDF15(hGDF15)
可直接评估人源抗体/蛋白药的靶向药效
表型可与“人源标志物-表型”相关性联动分析
H3:HT-1080 CDX模型——造模与表型
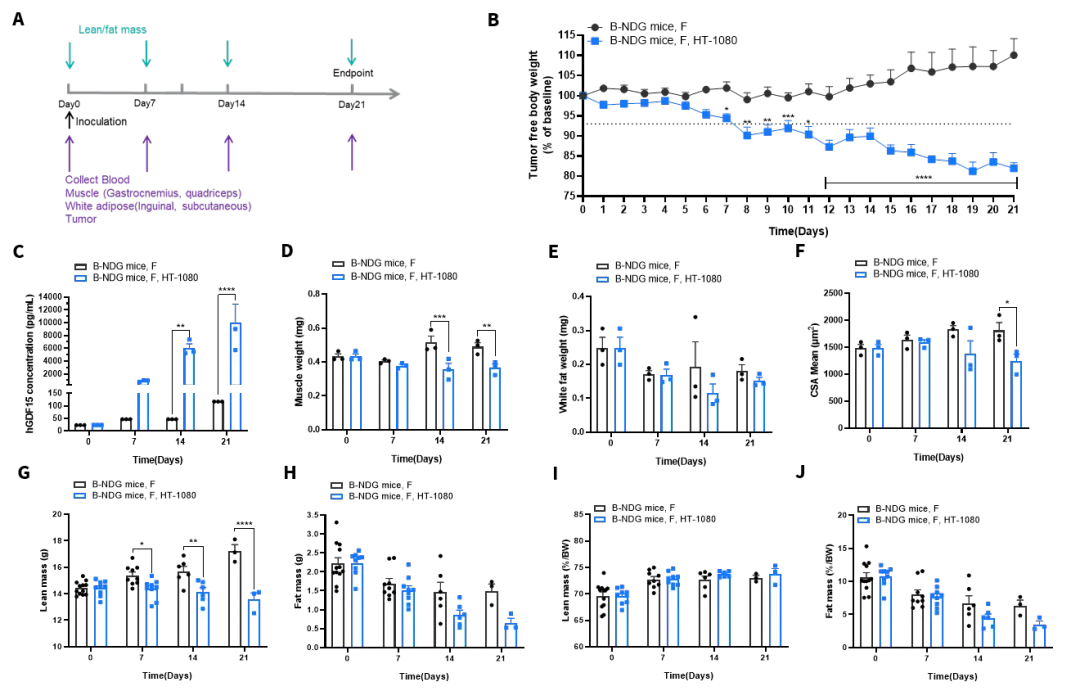
图7. CDX(HT-1080)诱导恶病质模型造模数据
图7A显示成功构建了HT-1080人源纤维肉瘤的CDX模型,并对其诱导的癌症恶病质表型进行了系统评估,证实该模型可引发显著的宿主消耗。如图7B所示,在肿瘤生长期间,小鼠的去瘤体重显著下降,表明发生了全身性的代谢消耗。通过血液检测发现,小鼠血浆中的人源GDF15(hGDF15)浓度急剧上升(图7C),证实HT-1080肿瘤持续分泌这一关键的恶病质驱动因子。骨骼肌重量(腓肠肌、股四头肌)显著减轻(图7D),白色脂肪组织(腹股沟、皮下)重量也明显减少(图7E),且骨骼肌的H&E染色切片显示,小鼠的肌纤维横截面积显著减小(图7F),从形态学上直接证实了肌肉萎缩的发生。模型小鼠的瘦体质量(Lean Mass)也显著下降(图7G)。
在成功建立 HT-1080诱导的恶病质模型后,,我们进一步开展了药效研究(图8)。小鼠在体重显著下降后(图8A,造模至分组前数据),被随机分为四个治疗组与对照组(保留未接种肿瘤细胞的小鼠为空白对照组),并接受为期两周的干预。
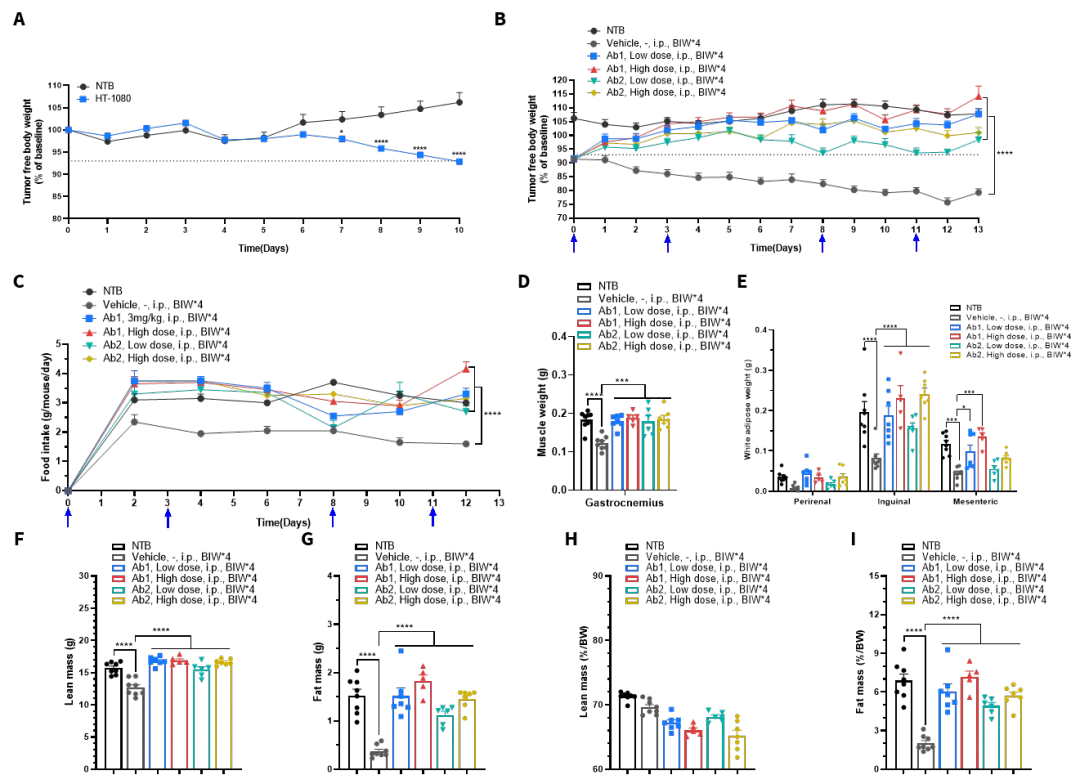
图8. CDX(HT-1080)诱导恶病质模型药效数据
治疗组小鼠给予hGDF15抗体(低或者高剂量,腹腔注射,每周两次,共计4次),对照组给予相应溶剂。干预期间持续监测体重变化,结果如图8B 所示,治疗组小鼠体重下降趋势得到明显缓解,表明有效改善体重丢失。图8C所示,治疗组小鼠摄食量显著高于对照组,表明改善体重丢失主要依靠增加小鼠食欲来实现的。
实验终点时,在体成分分析中治疗组小鼠的Lean mass与Fat mass较对照组均显著回升,骨骼肌(腓肠肌)重量也显著增加,白色脂肪组织(肾周、腹股沟、肠系膜)重量也显著上升。
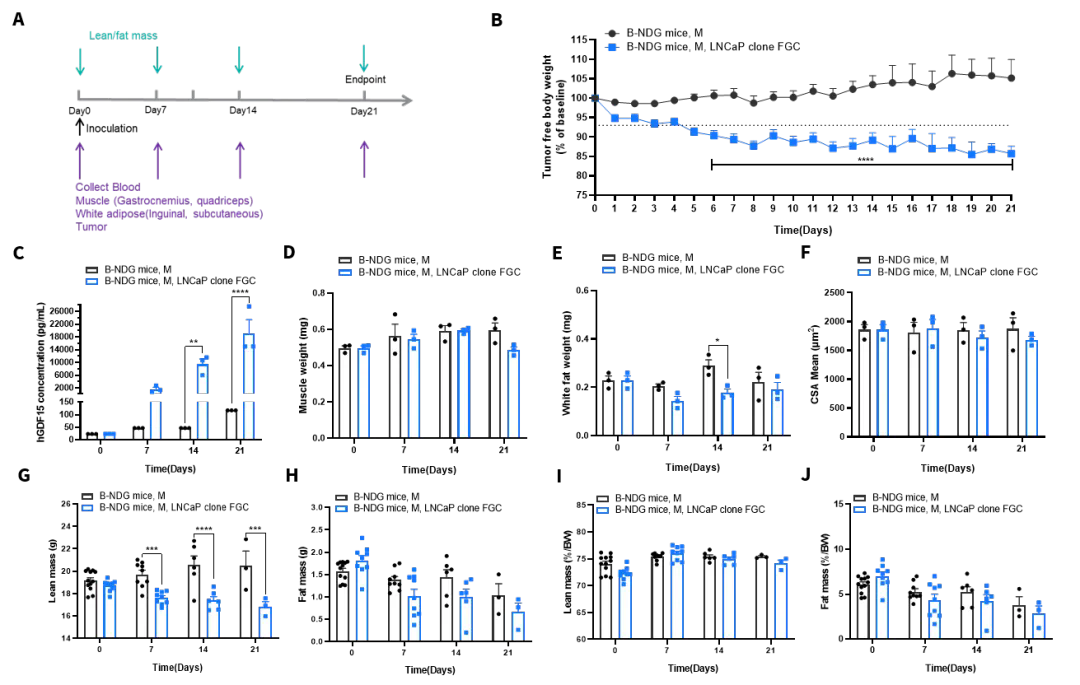
图9. CDX(LNCaP)诱导恶病质模型造模数据
此外,我们也成功构建了LNCaP人前列腺癌的CDX模型,并对其诱导的癌症恶病质表型进行了系统评估,成功诱导了显著的宿主消耗。如图9B所示,在肿瘤生长期间,小鼠的去瘤体重显著下降,表明发生了全身性的体重丢失。通过血液检测发现,小鼠血浆中的人源GDF15(hGDF15)浓度急剧上升(图9C),证实LNCaP肿瘤持续分泌这一关键的恶病质驱动因子。骨骼肌重量(腓肠肌、股四头肌)减轻(图9D),白色脂肪组织(腹股沟、皮下脂肪)重量也显著减少(图9E),且骨骼肌的H&E染色切片显示,小鼠的肌纤维横截面积也呈现减小趋势(图9F)。小鼠的瘦体质量(Lean Mass)显著下降(图9G)。
同样在成功建立 LNCaP诱导的恶病质模型后,我们进一步开展了药效研究(图10)。小鼠在体重显著下降后(图10B,造模至分组前数据),被随机分为治疗组与对照组(保留未接种肿瘤细胞的小鼠为空白对照组),并接受为期两周的干预。
治疗组小鼠给予 Ponsegromab(腹腔注射,每周两次,共计6次),对照组给予相应溶剂。干预期间持续监测体重变化,结果如图10C 所示,治疗组小鼠体重下降趋势得到明显缓解,表明有效改善体重丢失。
实验终点时,在体成分分析中治疗组小鼠的Lean mass与Fat mass较对照组均显著回升,白色脂肪组织(腹股沟、皮下)重量也显著上升。
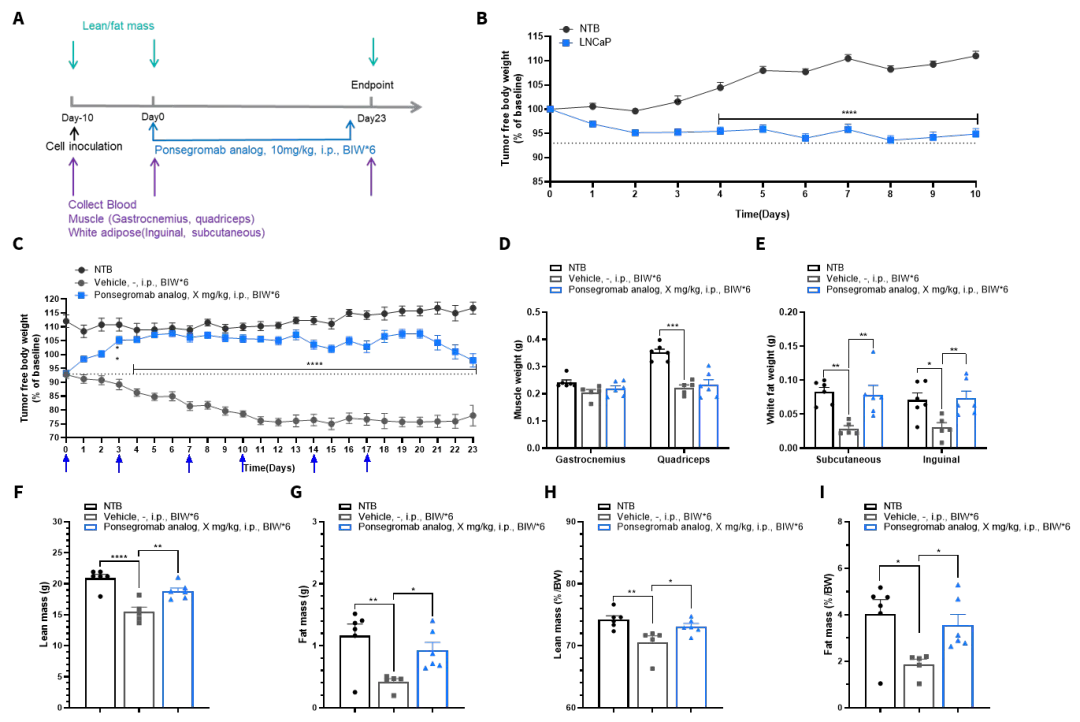
图10. CDX(LNCaP)诱导恶病质模型药效数据
综上所述,HT-1080和LNCaP CDX模型均能够全面模拟人类癌症恶病质的核心特征:伴随肿瘤生长,宿主出现进行性体重下降、循环GDF15水平升高、骨骼肌与脂肪组织的实质性丢失,以及体成分的恶化,给予hGDF15抗体药物后能提高食欲并全方位改善这些表型。该CDX恶病质模型是研究GDF15驱动型恶病质机制及评价相关疗法的理想临床前模型。
用“人源标志物(hGDF15)—摄食—体成分—组织终点”串联药效链路
同步呈现肿瘤生长曲线与去瘤体重,避免肿瘤负荷影响解释
对于食欲相关靶点,摄食量为关键的机制支持终点

参考文献:
1. Li L, et al. A comprehensive review of animal models
for cancer cachexia: implications for translational research. Frontiers in Oncology. 2023;13:1048657.
2. Fearon K, et al. Definition and classification of
cancer cachexia: an international consensus. The Lancet Oncology. 2011;12(5):489-495.
3. Fearon KC, et al. Cancer cachexia: mediators,
signaling, and metabolic pathways. Cell Metabolism. 2012;16(2):153-166.
4. Wakabayashi H, et al. The regulatory approval of
anamorelin for treatment of cachexia in Japan. Journal of Cachexia, Sarcopenia and Muscle. 2021;12(5):1273-1276.
5. Mueller TC, et al. Molecular pathways leading to loss
of skeletal muscle mass in cancer cachexia—can findings from animal models be translated to humans? BMC Cancer. 2016;16:75.
6. Chen G, et al. Bridging the tumor microenvironment:
the pivotal role of cancer-associated fibroblasts in tumor cachexia development. Molecular Cancer. 2025;24:194.
7. Wischhusen J, et al. Growth/Differentiation Factor-15
(GDF-15): From Biomarker to Novel Targetable Immune Checkpoint. Frontiers in Immunology. 2020;11:951.
8. Ahmed DS, et al. GDF15/GFRAL pathway as a metabolic
signature for cachexia in patients with cancer. Journal of Cancer. 2021;12(4):1125-1132.
9. Lerner L, et al. MAP3K11/GDF15 axis is a critical
driver of cancer cachexia. Journal of Cachexia, Sarcopenia and Muscle. 2016;7(4):467-482.