您可能也喜欢
药物通过口服、静脉注射和吸入等方式进入人体,但活性成分通常无法直接到达病变部位,无法发挥最大疗效。为了克服这一挑战,药物递送系统(Drug Delivery System,DDS)应运而生,帮助药物精准到达靶部位,并维持合适的浓度和作用时间。随着药学的进步与疗效安全性要求的提升,药物递送系统在药物研发中的重要性日益增加,尤其是在新药分子开发中,递送系统成为实现高效治疗的“最后一公里”。此外,药物递送技术的不断进展也为原本难以治疗的疾病带来了新的希望。
现代药物递送系统的起点可以追溯到1952年推出的Spansule®缓释胶囊,这种胶囊通过口服高分子包衣技术实现了12小时的缓释效果。此后,药物递送技术取得了长足发展。在1980年代,口服制剂和透皮制剂为小分子药物提供了长达24小时的缓释效果。进入1990年代,Lupron Depot®的推出使长效注射剂和植入剂得以广泛应用,将给药时间从几天延长至几个月。到了2000年代,纳米药物技术的迅猛发展加速了2020年新冠mRNA疫苗的研发和应用。同时,抗体偶联药物(ADC)技术成为当前抗肿瘤药物研发的热点[1]。
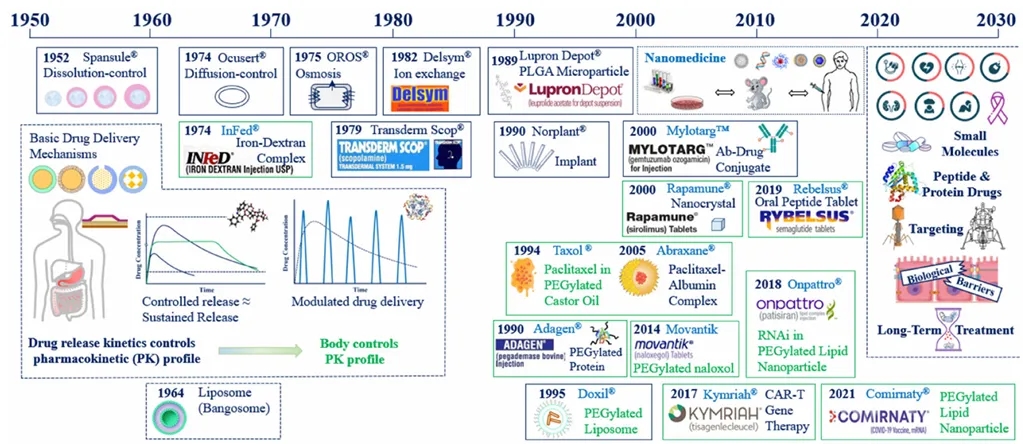
图1 药物递送系统的发展[1]
药物递送系统根据核心功能的不同,主要可以分为两大类:控释药物递送系统和靶向药物递送系统。
早期的药物递送系统主要集中在小分子化合物的控释制剂,通常用于口服制剂和透皮制剂,提供12小时或24小时的持续给药效果。随后,武田与雅培合作开发了首个长效注射剂——Lupron Depot®,它能够在一个月内缓慢释放醋酸亮丙瑞林。PLGA微粒制剂通过调整丙交酯与乙交酯的比例(L:G比)和聚合物分子量,将药物给药时间延长至6个月。此类长效注射制剂可用于小分子、肽类和蛋白质等药物的递送。代表性的长效注射制剂包括脂质体(如阿霉素脂质体Doxil®)、纳米颗粒(如紫杉醇-白蛋白复合物Abraxane®)、纳米晶体(如西罗莫司纳米晶制剂Rapamune®)以及脂肪乳(如阿瑞匹坦注射用乳剂Cinvanti®)等。
近年来,靶向药物递送成为药物递送系统开发的核心方向,涵盖了偶联靶向递送、纳米脂质体靶向递送和仿生靶向递送等技术。
纳米脂质体靶向递送系统通常可分为三类[2]:
被动靶向:通过调节纳米颗粒的物理特性(如大小、形状、硬度和表面电荷),使其在解剖学和生理学的基础上实现自然靶向。
主动靶向:利用化学或生物方法修饰纳米颗粒表面,使其特异性地与靶器官高度表达的受体结合,完成精准递送。
内源性靶向:通过调整纳米颗粒的组成,使其与血液中的特定血浆蛋白结合,从而引导药物到目标器官,并促进特定细胞的摄取。
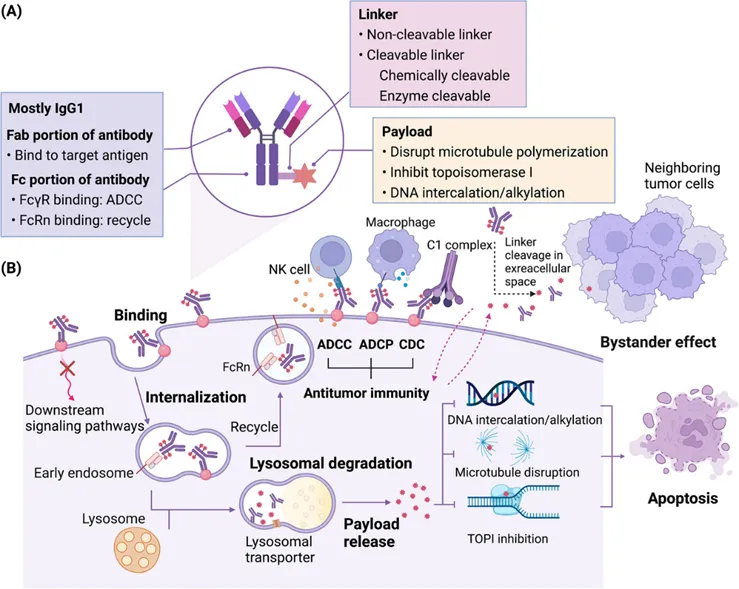
图2 ADC药物作用机制图示[3]
以抗体偶联药物(ADC)为代表的偶联靶向递送技术发展迅速。最初的设计思路是将靶向抗体与药物分子通过化学键连接,形成创新药物,具备主动靶向递送的能力。随着ADC研究的深入,其设计理念已经超出了简单的药物递送。例如,DS-8201使用的Her2单抗不仅能靶向递送小分子毒素,还具有抗肿瘤活性。
此外,研究者也在积极探索包括多肽偶联药物(PDC)、核素偶联药物(RDC)、抗体细胞偶联药物(ACC)、抗体片段偶联药物(FDC)、抗体寡核苷酸偶联物(AOC)、抗体免疫刺激偶联物(ISAC)等多种递送功能药物,推动药物递送系统的多元化发展。
对于中枢神经系统疾病,如何突破血脑屏障(BBB)是一个长期存在的难题。利用药物偶联靶向递送技术穿越血脑屏障,已成为神经科学领域的重要研究方向。此类技术为相关疾病的治疗带来了新的希望,尤其是对于阿尔茨海默病等神经退行性疾病的治疗。
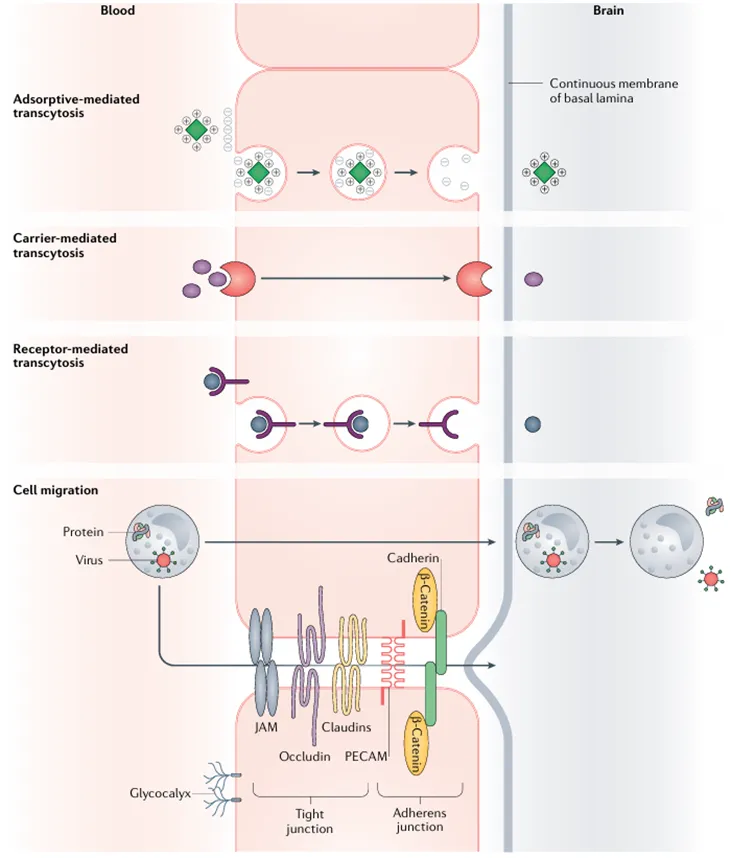
图3 常见跨血脑屏障的递送技术[4]
目前,多个平台已经实现了通过TFR1载体将药物送过血脑屏障。代表性平台包括Bioarctic公司的Brain Transporter™[5]、罗氏的Brainshuttle™[6]和Denali的Transport Vehicle(TV)[7]等。
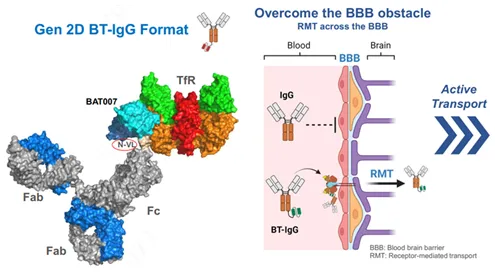
图4 Bioarctic公司的BrainTransporter™[5]
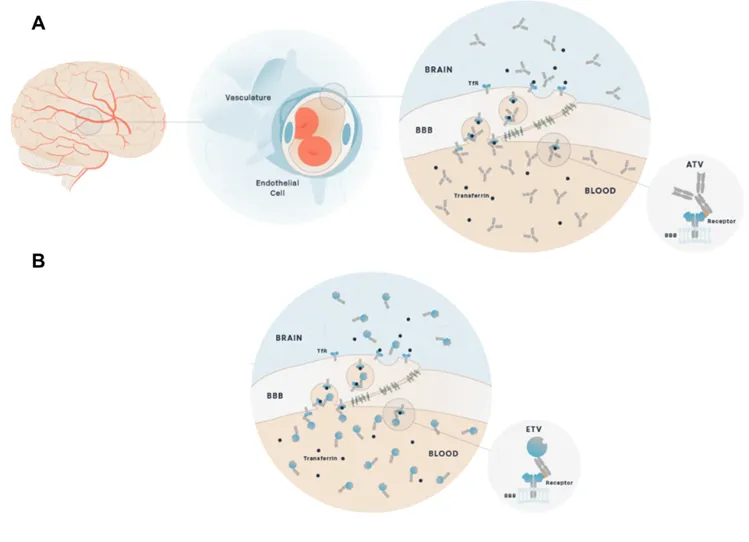
图4 Denali的Antibody Transport Vehicle(ATV)和Enzyme Transport Vehicle(ETV)[7]
CD98hc是新药开发中脑部递送的热门靶标。研究发现,以CD98hc为载体的生物大分子递送系统,虽然摄取速度较TFR1慢,但能够显著延长药物在大脑中的暴露时间,并展现出独特的脑内分布模式,具有广阔的应用前景[8]。
药物递送系统作为药物开发的关键环节,经过70多年的发展,已取得了显著的进步。随着多学科的交叉研究不断深入,药物递送系统有望实现更高效、精准的治疗,为全球健康需求提供有力支持,推动医药产业的可持续发展。
针对TFR1和CD98hc靶点的研究以及新药开发需求,百奥赛图公司开发了TFR1人源化鼠和CD98hc人源化鼠。
B-hTFR1小鼠相关数据
利用光片荧光显微镜检测脑内抗体
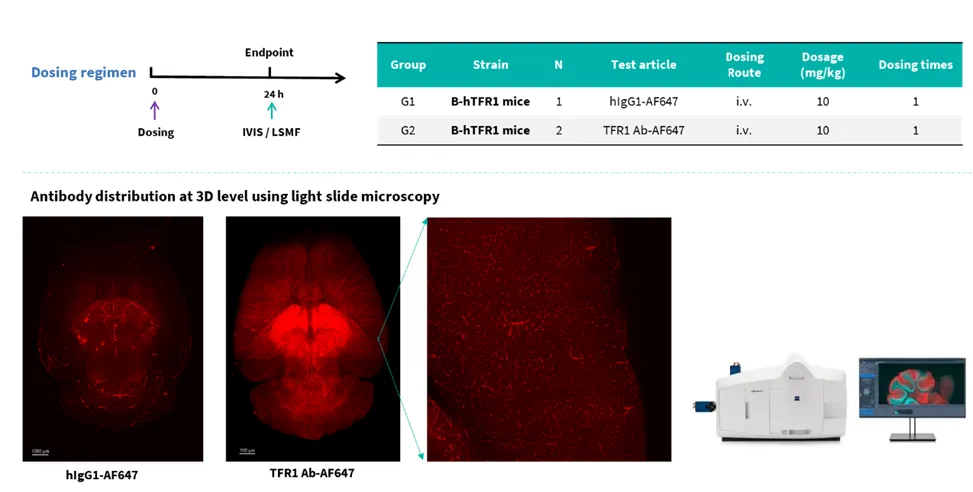
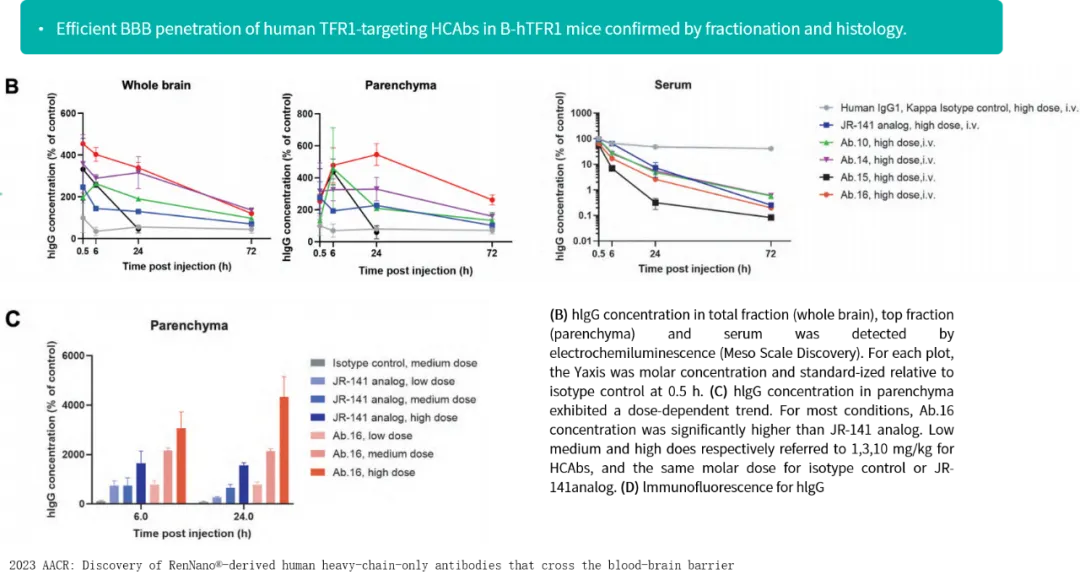
人源化单抗在血脑屏障中的穿透情况
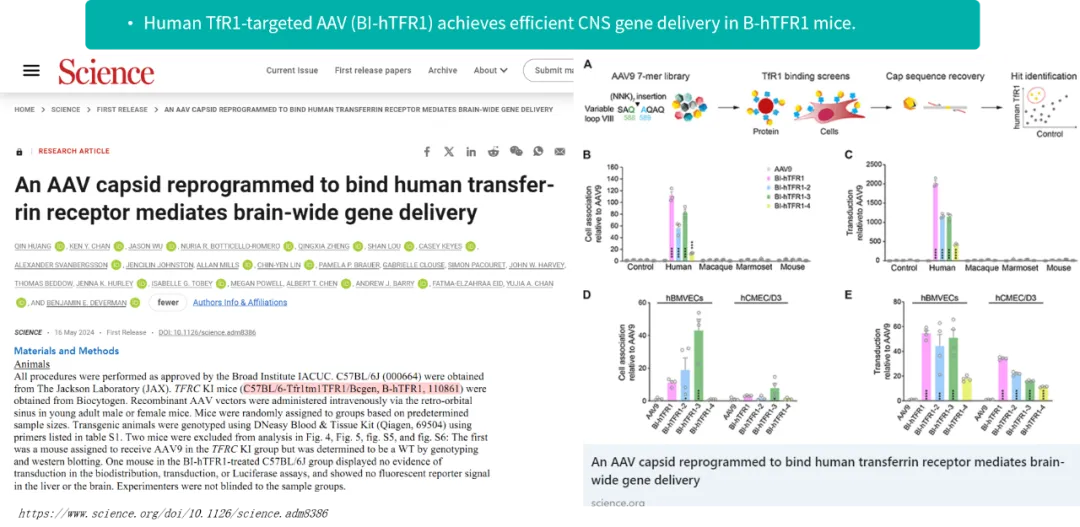
人TfR1靶向型AAV在血脑屏障中的穿透情况
B-hTFR1/hDMPK小鼠相关数据
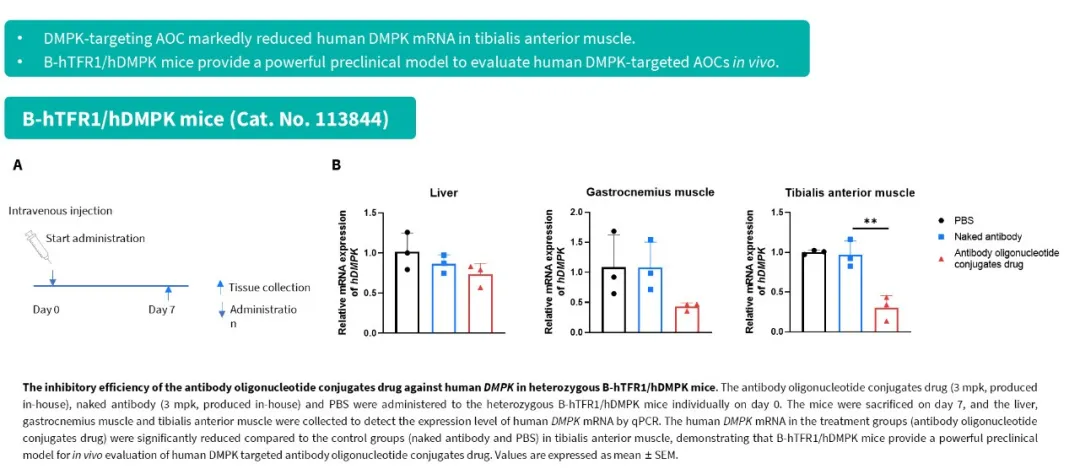
TFR1介导的肌肉部位药物输送
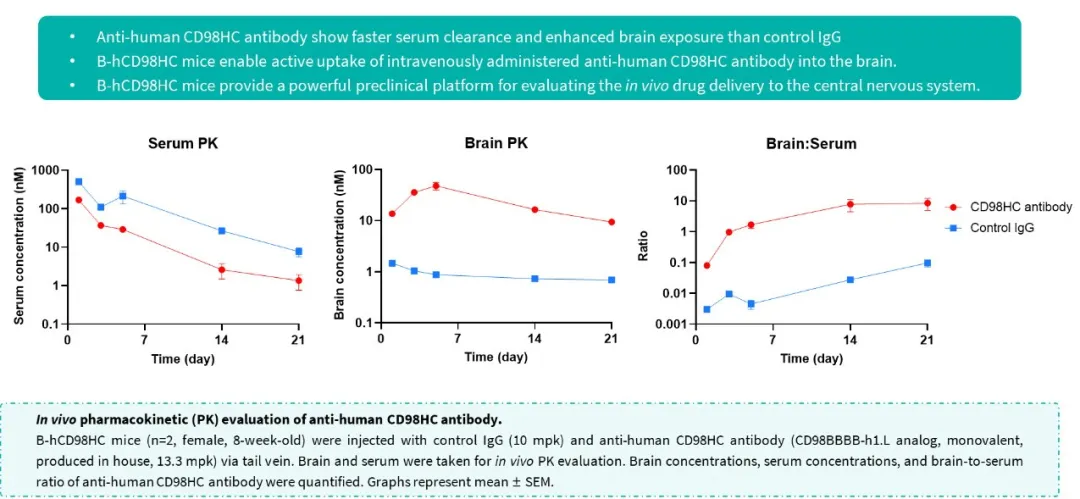
B-hCD98HC小鼠相关数据
抗人CD98HC抗体在大脑中的有效摄取
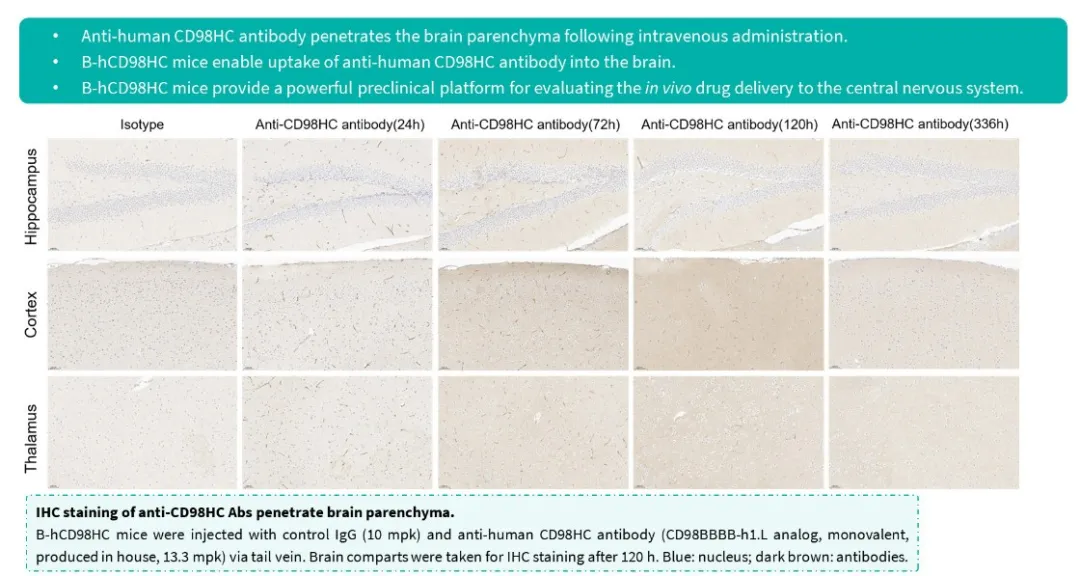
抗人CH98HC抗体能够穿透脑实质组织
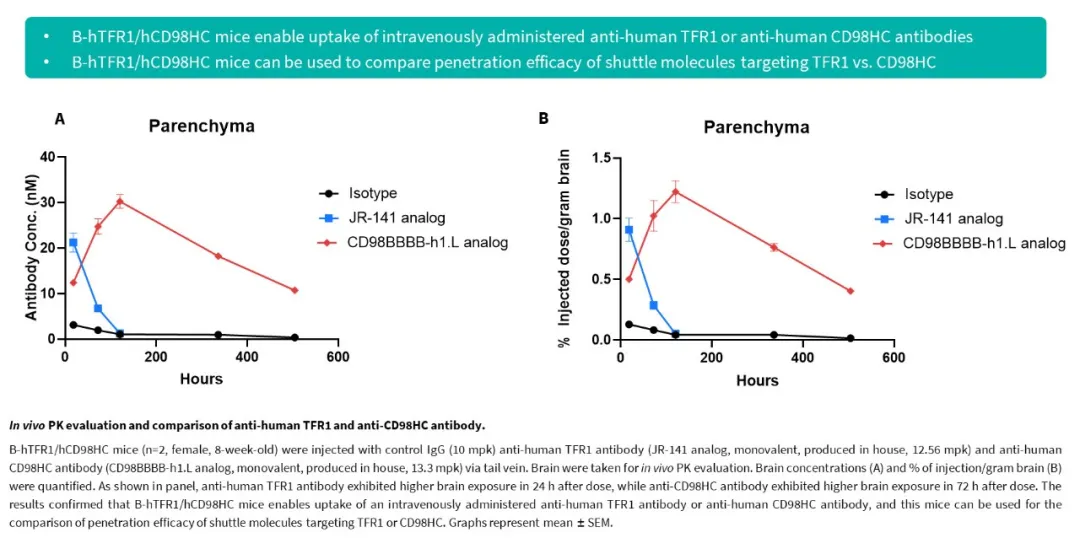
B-hTFR1/hCD98HC小鼠相关数据
抗人TFR1与CD98HC抗体体内PK评估与比较
参考文献
[1] Park H, Otte A, Park K. Evolution of drug delivery systems: From 1950 to 2020 and beyond. J Control Release. 2022 Feb;342:53-65. doi: 10.1016/j.jconrel.2021.12.030. Epub 2021 Dec 29. PMID: 34971694; PMCID: PMC8840987.
[2] Dilliard SA, Siegwart DJ. Passive, active and endogenous organ-targeted lipid and polymer nanoparticles for delivery of genetic drugs. Nat Rev Mater. 2023;8(4):282-300. doi: 10.1038/s41578-022-00529-7. Epub 2023 Jan 19. PMID: 36691401; PMCID: PMC9850348.
[3] Chen YF, Xu YY, Shao ZM, Yu KD. Resistance to antibody-drug conjugates in breast cancer: mechanisms and solutions. Cancer Commun (Lond). 2023 Mar;43(3):297-337. doi: 10.1002/cac2.12387. Epub 2022 Nov 10. PMID: 36357174; PMCID: PMC10009672.
[4] Terstappen, G.C., Meyer, A.H., Bell, R.D. et al. Strategies for delivering therapeutics across the blood–brain barrier. Nat Rev Drug Discov 20, 362–383 (2021). https://doi.org/10.1038/s41573-021-00139-y
[5]https://www.bioarctic.com/en/wp-content/uploads/sites/ 2/2024/12/BrainTransporter-presentation-November-2024-PEGS-Barcelona.pdf
[6]https://medically.roche.com/global/en/neuroscience/adpd-2024/medical-material/ADPD-2024-presentation-kulic-rapid-dose-dependent-amyloid-plaque-pdf.html
[7] https://www.denalitherapeutics.com/science/engineering
[8] Chew KS, Wells RC, Moshkforoush A, Chan D, Lechtenberg KJ, Tran HL, Chow J, Kim DJ, Robles-Colmenares Y, Srivastava DB, Tong RK, Tong M, Xa K, Yang A, Zhou Y, Akkapeddi P, Annamalai L, Bajc K, Blanchette M, Cherf GM, Earr TK, Gill A, Huynh D, Joy D, Knight KN, Lac D, Leung AW, Lexa KW, Liau NPD, Becerra I, Malfavon M, McInnes J, Nguyen HN, Lozano EI, Pizzo ME, Roche E, Sacayon P, Calvert MEK, Daneman R, Dennis MS, Duque J, Gadkar K, Lewcock JW, Mahon CS, Meisner R, Solanoy H, Thorne RG, Watts RJ, Zuchero YJY, Kariolis MS. CD98hc is a target for brain delivery of biotherapeutics. Nat Commun. 2023 Aug 19;14(1):5053. doi: 10.1038/s41467-023-40681-4. Erratum in: Nat Commun. 2023 Sep 7;14(1):5516. doi: 10.1038/s41467-023-41355-x. PMID: 37598178; PMCID: PMC10439950.